热线:021-66110819,13564362870
Email:info@vizai.cn


热线:021-66110819,13564362870
Email:info@vizai.cn
来自英国剑桥大学的George G.Malliaras团队利用软机器人致动器和柔性电子器件的最新进展,开发出了高度保形的神经袖带,它将电化学驱动的导电聚合物软致动器与低阻抗微电极结合在一起。这些袖套在小至几百毫伏的外加电压驱动下,可以主动抓取或包裹脆弱的神经。本研究利用体内大鼠模型对这项技术进行了验证,结果表明,这种袖套无需使用手术缝合线或胶水,就能与大鼠坐骨神经形成并保持自闭合和可靠的生物电子界面。这种软电化学致动器与神经技术的无缝整合为实现术中微创神经活动监测和高质量生物电子接口提供了一条途径。相关工作以题为“Electrochemically actuated microelectrodes for minimally invasive peripheral nerve interfaces”的文章发表在2024年04月26日的国际顶级期刊《Nature Materials》。
设计
本研究开发了软机器人、薄膜生物电子外周神经袖带,它集成了数十个分布式高分辨率微电极和基于导电聚合物的双层致动器,可通过可编程的电子输入进行控制。
本研究的软机器人外周神经袖带由微图案致动元件组成,可按需进行形状变形,周围是分布式电生理学电极。图1a展示了两幅插图:一幅描绘了轻柔地握住神经的过程,而另一幅则展示了围绕神经的螺旋缠绕。后一种方法能够适应不同直径的神经,避免了传统袖带因电极-神经束排列不整齐而经常出现的通信问题。致动器本质上是电子元件,与微电极阵列采用相同的光刻制造工艺。这种无缝集成为设计致动器的形状和分布留出了空间,以满足定制的形状变化需求。
例如,致动器元件的垂直排列最大限度地减少了向垂直方向的弯曲,只允许沿着电极的排列方向进行大的弯曲,可实现的弯曲半径小至170微米(图1b)。值得注意的是,通过设计致动器元件的非对称分布实现了螺旋包裹神经袖带。
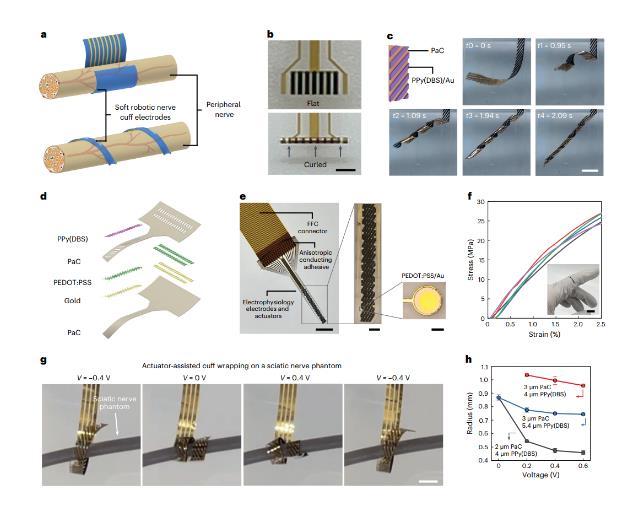
如图1c所示,倾斜Au/PPY(DBS)元件的集成使原始形状迅速转变为螺旋结构,在2.1秒内形成四圈。然后,利用这种不对称结构构建了螺旋可驱动神经袖带。图1d是袖带的剖视示意图。装置的整体结构如图1e所示,放大的光学显微照片提供了致动器和微电极阵列的细节。
定制接口部分包括致动器和微电极,宽度为2.1毫米,长度为10.7毫米。特别值得一提的是,所有功能元件都共用一套柔性电触点和连接线,无需使用传统致动机构中常见的复杂而坚固的控制元件。这种简化减少了机械不匹配的风险,有利于微型化进程。在静态拉伸测试中(图1f),薄层结构显示出1.24 GPa的模量,与PaC的模量(1.13 GPa)非常接近,表明薄金属层对模量的影响微乎其微。
尽管基于PaC的设备比神经组织更坚硬,但其超薄的外形却赋予了其显著的灵活性。
本研究使用从Föppl–von Kármán板理论中推导出的模型估算了它们的弯曲刚度。得出的弯曲刚度为21 Pa mm3,相当于厚度为11.4μm的单层PPy(DBS)或厚度为40.0μm的单层聚二甲基硅氧烷。这种低刚度有效地解决了植入物与组织之间的机械不匹配问题,促进了更亲密、更稳定的界面,大大降低了组织损伤引起的异物反应。使用简化的装置验证了袖带在体外自我包裹神经的能力,该装置包括将一根绝缘导线作为坐骨神经模型浸没在PBS溶液中,并置于琼脂糖凝胶上。
导线和凝胶之间保持很小的间隙,允许装置穿过。如图1g所示,逐步施加-0.4至0.4 V的电压时,装置缓慢缠绕假体并逐渐收紧,直至形成牢固的抓握,并在施加-0.4 V电压时松开。装置的缠绕半径由PaC层和PPy(DBS)层的厚度控制(图1h)。
验证
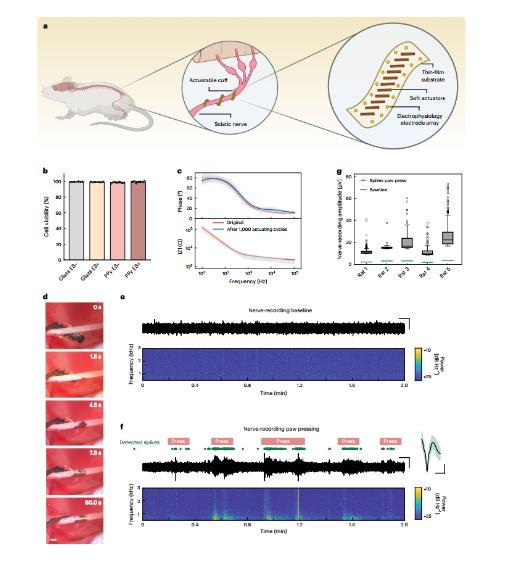
本研究选择了2微米厚的PaC和4微米厚的PPy(DBS)组合作为最终设计,并在大鼠坐骨神经上进行了体内验证,其中集成了28个聚(3,4-亚乙二氧基噻吩)聚苯乙烯磺酸盐(PEDOT:PSS)/金微电极,用于记录神经活动(图2a)。为了在体内验证前评估PPy(DBS)的细胞活力,使用播种在PPy(DBS)上的SH-SY5Y细胞和作为对照的玻璃载玻片进行了活/死细胞检测。所有PPy(DBS)样品都表现出显著的细胞活力,细胞活力值约为99%,与玻璃载玻片上的对照组相似(图2b)。此外,在电生理学微电极中加入PEDOT:PSS后,阻抗很低(在PBS中1 kHz时为4.1±0.4 kΩ),即使经过1,000次大的弯曲循环,阻抗的增加也可以忽略不计(图2c)。
总结与展望
将软电化学致动器集成到薄膜生物电子学中,可为微创神经连接手术提供一种新型的柔性。利用传统的微细加工技术,本研究制备了将精确图案化的致动器元件和微电极阵列集成在单一结构中的薄膜设备。这种电力驱动的软机器人电极无需额外的笨重和刚性致动器以及其他方法中常用的复杂控制系统。凭借溶解阳离子在外加电压作用下的可逆传输,实现了形状转换。为确保在生物医学领域的安全使用,本研究已将致动所需的电压大幅降至极低值。虽然这可能会导致较低的致动力,但微米厚的薄膜结构却能产生理想的较大致动应变。本研究通过设计致动元件的分布,展示了不同的形状变换模式。此外,打破结构对称性还可以实现复杂的螺旋形状。本研究强调,必须精心设计每一层的厚度,以优化特定应用设置的性能。