热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
研究简介:铁是地壳中最丰富的氧化还原活性元素。硝化-还原铁(II)-氧化细菌已经知道大约20年了。在多大程度上降低硝酸盐和铁的氧化是通过酶的途径或由异养反硝化形成的亚硝酸盐引起的非生物过程这个结论,已经引起了许多争论。到目前为止,唯一已知的实验室可以长期维持培养的是culture KS,这种纯具有自养硝酸盐还原Fe(II)氧化能力的培养物,然而能够连续Fe(II)氧化和自养的能力的微生物代近些年来还未培养出来,只是在近几年在沿海海洋沉积物中,还发现了自养硝酸盐还原铁(II)-氧化细菌的存在。
本论文研究的目的是通过监测底物浓度和活性的变化来评估硝酸盐还原和铁(II)氧化的耦合,以及对天然浅海淡水沉积物中的硝化细菌的活性对硝酸盐和铁的刺激(II)的影响。
Unisense微电极系统的应用
应用了溶氧微电极OX-100,氧化还原电极以及PH-100三种微电极对康斯坦斯湖沿岸所取的沉积物柱芯样品的氧、pH、氧化还原电位等进行了原位测试,其中对在所取的沉积物测量之前和测试期间,在沉积物中覆盖的水进行曝气,这是为了还原海洋种的表面沉积物中是充满了氧气的。对于沉积物中的氧的微剖面测试采用的是手动微推进器,每次测试步径为200微米。而对于氧化还原电位以及pH的微剖面测试采用的测试步径是500微米。
实验结果
研究发现在经过改良的微生态系统中。铁的生物氧化依赖于微生物同步还原硝酸的过程,此外还发现亚硝酸盐在经过消毒的沉积物中,亚硝酸盐的非生物氧化反应速度不足以解释在微生物活性沉积物中观察到的铁氧化速率。此外酶的基因编码的表达水平对硝酸盐还原至关重要,尤其受到了环境中二价铁的刺激作用。这些结果表明,二价铁对细菌的反硝化作用有直接的影响,并支持了微生物硝酸盐的减少是由生物铁(II)氧化引起的的假说。
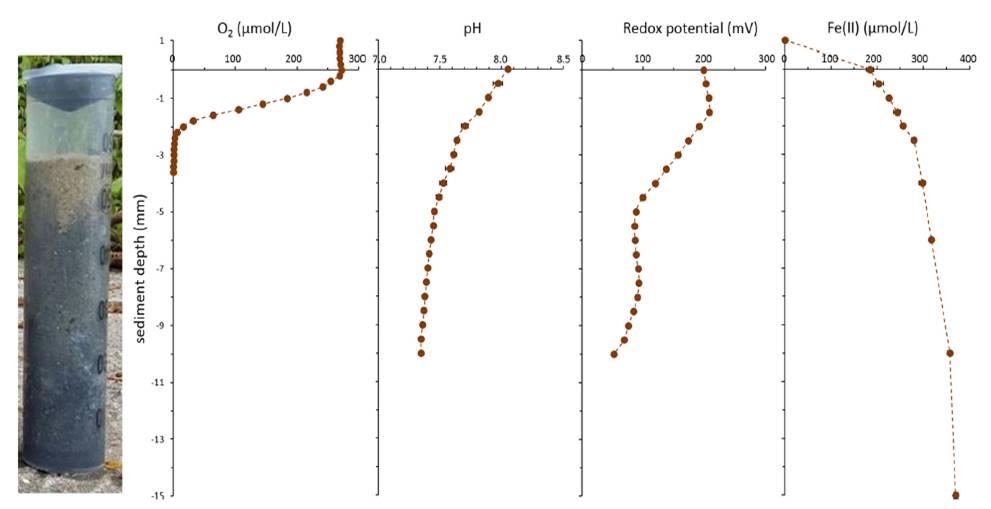
图1、康斯坦斯湖沿岸沉积岩心中测试的氧,pH,氧化还原电位,和Fe(II)的剖面图。从图中可以看出,所取的海洋沉积物中的氧的浓度是随着距离界面越远,其氧的浓度最近降低,大约在界面下4mm处体系中的氧浓度几乎为零。对于沉积物岩心中的pH值也是随着沉积物界面处的深度增加表现为不断变小。而对于氧化还原电位值表现为先减小后并最后稳定120mv,但是体系中的二价铁则表现为随着距离沉积物界面处的距离增加,其二价铁的浓度逐步增加。
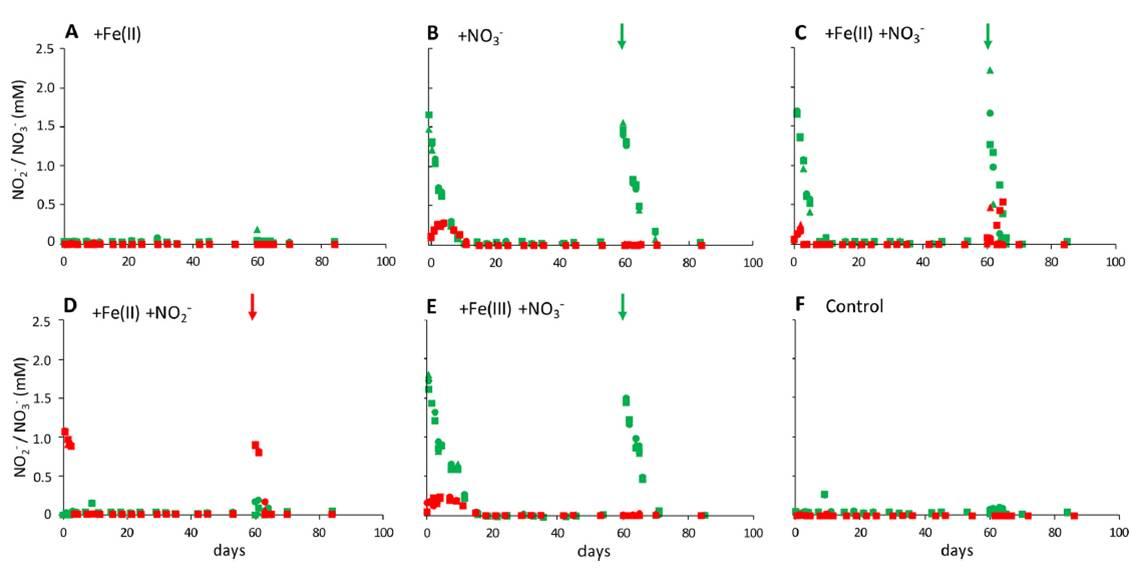
图2、在不同的微观环境中测试的硝酸盐(绿色)和亚硝酸盐(红色)的浓度(三角形、正方形和菱形符号分别代表了三倍体系的浓度)。体系中更正的浓度(5 mM的Fe(II)和Fe(III)除了从沉积物中衍生出1mM,2mM来自于硝酸盐和亚硝酸盐),微观环境的加入表示的是加入硝酸盐或亚硝酸盐后第60天。

图3、亚硝酸盐浓度(红色)和Fe(II)/Fe(tot)比率(灰色)在生物(填充的符号)和非生物(空心结构符号)随着时间的变化情况(三角形,正方形,和钻石符号显示的三倍体系)。其中在初始修正后的Fe[II]浓度为5 mM,亚硝酸盐浓度为2 mM,微观体在第60天(见箭头)加入亚硝酸盐后呈现的体系浓度情况。
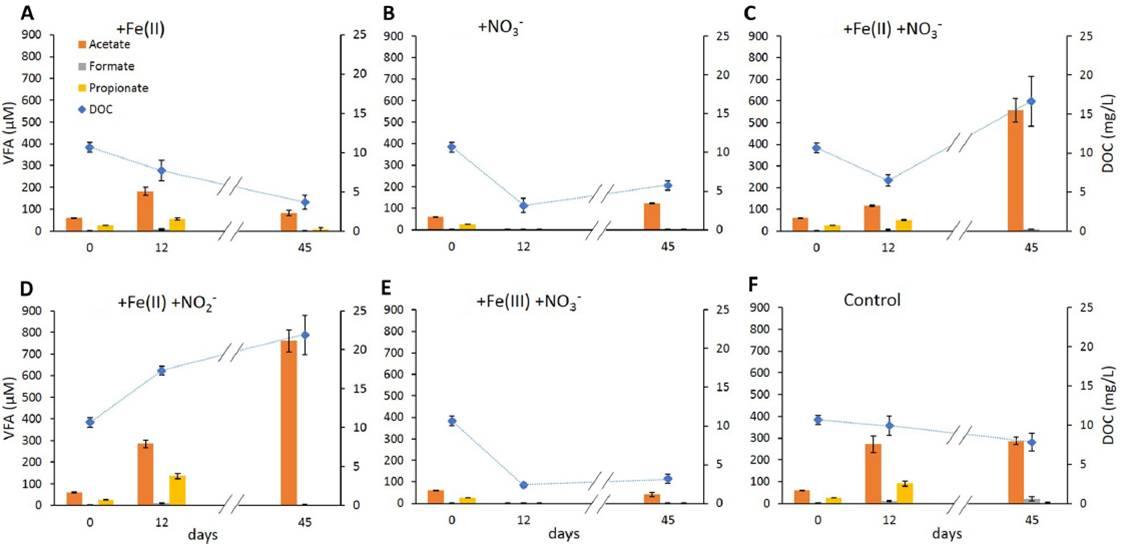
图4、随着时间的推移,体系中溶解的有机碳(蓝色钻石符号)和挥发性脂肪酸(棒)的浓度在设置的不同微观环境体系中随时间的变化情况。
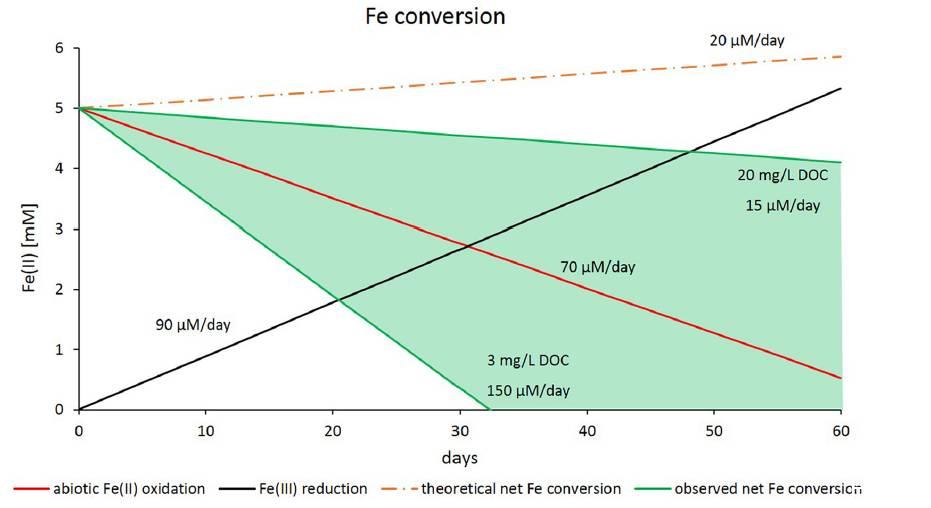
图5、铁的转化率(同步显示的净利率,其中Fe[II]氧化和Fe[III]的还原都依赖于DOC的浓度。选用5mM的Fe(II)或Fe(III)和2mM的硝酸盐或亚硝酸盐进行的微观实验的相关测试。理论铁的转换率显示了Fe(II)的氧化反应只与亚硝酸盐的反应有关的假设。理论Fe的转换率(橙色虚线)与实测Fe的转化率区别。
总结
本论文主要就沿海沉积物中的Fe(II)氧化与硝酸盐还原进行相关研究,之前的很多研究认为,沉积物中的Fe(II)氧化对硝酸盐还原的依赖性导致了两个过程都是酶耦合的结论,但是结合实际观察却发现,普通的硝酸盐还原菌可以通过反应性氮素,在非生物的条件下氧化Fe(II)。在反硝化过程中观察到的这些结果引起了相关科研人员对于体系中的硝酸盐还原与Fe(II)氧化的耦合酶是否存在产生怀疑,本论文基于此项研究的疑虑,结合使用了unisense微电极研究系统实现了原位的测试沉积物中的Fe(II)、氧气、pH、氧化还原电位等相关参数,提出了沉积物中硝酸还原铁(II)氧化的基本机理,并且得出了Fe(II)氧化与硝酸盐还原反应主要是一种微生物介导的过程。这说明微电极在研究海洋沉积物氮循环机理方面存在着非常好的应用前景。
 相关新闻
相关新闻