热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
摘要:肠道微生物-肠-脑轴因其在调节精神疾病中的可能生物学基础作用而受到越来越多的关注。肠道微生物与抑郁症等精神疾病密切相关,肠道微生物可通过与“肠-脑轴”交互作用影响抑郁症的发生和发展,然而,肠道微生物与抑郁症之间的具体相互作用及机制还未十分明晰。深入研究微生物-肠-脑轴和抑郁症之间的相互关系,有助于我们从另一个角度更为深刻地认识和阐明抑郁症这种精神疾病。调节肠道微生物组成来治疗、预防抑郁症等精神疾病是今后的研究方向之一,可为探索中医药治疗、预防抑郁症机理提供新的思路。
抑郁症是心境障碍的一种主要形式,具有高发病率、高自杀率和高复发率的特点[1]。流行病学研究发现,全世界约有3.5亿人患有抑郁症,并且这一数字逐年增加,根据全球疾病负担研究的结果,因抑郁症导致的伤残损失健康生命年(years lost to disability,YLD)在世界十大致残疾病中排名第一,抑郁症已成为全球致残的主要原因,也是日益严重的公共卫生问题[2]。抑郁症的发病原因尚不清楚,发病机制复杂,涉及遗传、生物、心理和社会环境等众多因素,主要与下丘脑-垂体-肾上腺(hypothalamic-pituitary-adrenal axis,HPA)轴功能失调、神经营养因子、氧化应激和炎症细胞因子失衡等生物学机制有关,但目前学界普遍认为,5-羟色胺、去甲肾上腺素和多巴胺或受体的异常表达是抑郁症的主要发病机制[3-4]。目前研究表明,抑郁症与个体肠道微生物密切相关,肠道微生物可以介导神经(神经递质)、内分泌(激素)、免疫(细胞因子)、代谢等途径,与大脑进行双向调节,这种双向调节作用的通道被称为微生物-肠-脑轴(microbiota-gut-brain axis,MGB);大脑可以通过微生物-肠-脑轴来改变肠道微生物的结构和多样性,肠道微生物菌群也可以通过肠脑轴来调节脑功能、情绪及焦虑相关的行为[5]。微生物-肠-脑轴失衡可影响行为表型,导致神经精神疾病[6]。肠道微生物改变及随之的肠-脑轴功能异常是抑郁症发生的病理基础,调节肠道微生物可能是预防和治疗抑郁症的有效方法[7-8]。因此,本文希望通过对微生物-肠-脑轴相关的中西医研究新进展进行总结,为肠道微生物对抑郁症的调控寻找更多的证据,为中医药通过微生物-肠-脑轴调控抑郁症的机制研究提供理论依据。
1、微生物-肠-脑轴
肠道微生物又称肠道菌群或肠道微生态,肠道微生物生物量占人体微生物总生物量的78%,在人体内大约有400−500种肠道细菌,主要由厚壁菌门、拟杆菌门、变形菌门、放线菌门等正常肠道菌群构成[9]。结肠内寄居着人体消化道内大部分的正常微生物群,最新估计肠道微生物的数量为4×1013个以上,对人体有益的微生物主要是双歧杆菌的部分菌属、乳酸菌等[10]。肠道微生物中的某些特定微生物具有独特的功能,有的能够预测肠道微环境,如阿克曼菌丰度增加则提示黏液层厚度提高、肠道通透性降低[11]。微生物-肠-脑轴的研究表明,肠道微生物群在协调大脑发育和行为方面发挥着关键作用[12]。在焦虑、抑郁、认知和自闭症谱系障碍中,肠道和大脑之间存在着交流。肠道微生物群在血脑屏障的形成、髓鞘形成、神经发生和小胶质细胞成熟等基本神经生成过程中发挥作用,并调节动物行为的许多方面[13]。胃肠道中的细菌,包括共生菌、益生菌和致病菌可以激活神经通路和中枢神经系统信号系统[14]。肠道微生物可能作为微炎性反应状态的启动者,介导肠道稳态失衡,进而导致“微生物-肠-脑轴”功能紊乱,在抑郁症的发病中扮演重要的角色[15]。
2、抑郁症患者肠道微生物的特点
抑郁状态可能诱导特定肠道微生物群物种的改变,并最终导致更严重的抑郁症。大脑可以通过微生物-肠-脑轴影响抑郁症肠道菌群的物种组成多样性及其丰度变化。对抑郁症患者粪便样本进行分析所产生的数据表明,抑郁症和粪便微生物群之间存在关联性[16]。一项研究发现,抑郁症患者组(46名)比健康对照组(30名)粪便细菌α多样性增加[17]。有研究表明,抑郁症人群肠道乳杆菌和双歧杆菌数量显著减少,肠杆菌科及肠球菌细菌数量显著增加[18]。也有研究表明,抑郁症患者病情严重程度与抗炎性细菌拟杆菌属和栖粪杆菌属丰度成反比,与毛螺菌属丰度成正比[19]。重度抑郁症患者和健康对照的肠道微生物组合物与重度抑郁症患者显著不同,重度抑郁症患者的特征在于厚壁菌门、放线菌和拟杆菌相对丰度的显著变化[20]。通过16S rRNA基因测序对36名重度抑郁症患者和37名健康对照者的研究发现,23个分类微生物群(4个门、7个家族和12个属)与抑郁症相关;在重度抑郁症患者中,放线菌门和厚壁菌门的比例过高;在属水平上,重度抑郁症患者中双歧杆菌(7%)和劳特氏菌属(8%)的丰度较高,而对照组中普雷沃菌属(16%)的丰度较高[21]。
3、肠道微生物影响抑郁症的发生发展
肠道微生物可以通过微生物-肠-脑轴作用于大脑,而特定物种的肠道微生物群体的改变可能导致抑郁[22]。抑郁症的发病与神经递质密切相关,而肠道微生物影响情绪也可能与神经递质密不可分,如:链球菌、肠球菌、埃希菌属可产生5-羟色胺;埃希菌、杆菌、酵母菌可合成去甲肾上腺素[23]。在一项随机双盲对照试验(n=544)中,对使用6周的长双歧杆菌NCC3001治疗患者,通过功能性磁共振成像(functional magnetic resonance imaging,fMRI)研究表明其可减弱对杏仁核和额叶边缘区域负性情绪刺激的反应,并降低了医院焦虑和抑郁量表的抑郁分值[24]。酪酸梭菌MIYAIRI 588联合抗抑郁药对治疗抵抗性重度抑郁症有效且耐受性良好[25]。
鼠李糖乳杆菌长期治疗可以减少前额皮质和杏仁核中γ-氨基丁酸(γ-aminobutyric,GABA)(Aα2)的信使核糖核酸(messenger RNA,mRNA)表达,增加海马中的GABA(Aα2),并且,鼠李糖乳杆菌可以减少应激诱导的皮质酮和焦虑、抑郁相关的行为[26]。小鼠粪便样品中的乳杆菌水平与应激诱导的抑郁样行为相关,而抑郁样症状则通过其代谢产物犬尿氨酸的治疗得到改善[27]。从抑郁患者和对照的亚组制备粪便微生物移植,并通过口服强饲法转移至微生物缺陷的大鼠模型,观察到来自抑郁患者的粪便微生物群移植可以诱导受体动物的抑郁症行为和生理特征,包括快感缺乏和类似焦虑的行为,以及色氨酸代谢的改变,说明通过肠道微生物转移可以重现抑郁行为和生理学方面的问题,提示肠道微生物可能在抑郁症发生的复杂机制中发挥因果作用[28]。
4、肠道微生物在抑郁症发生中的潜在机制
目前还没有一种完整阐明抑郁症发生机制的理论,肠道微生物在抑郁症发生中的机制主要有:单胺类神经递质失衡、炎症反应、HPA轴、神经营养因子失衡等[29]。抑郁情绪可以通过应激反应来改变机体的肠道通透性、破坏肠道粘膜屏障、激活肠黏膜免疫并导致肠道菌群结构紊乱,从而引起炎症反应[30]。将差异肠道细菌与抑郁症和差异代谢物的指标结合起来的研究发现,阿克曼菌、颤螺菌、瘤胃球菌、狄氏副拟杆菌、球杆菌和考拉杆菌属的改变与抑郁症状和炎性细胞因子的异常密切相关,而且,这些细菌与精氨酸、脯氨酸代谢和乙醛酸、二羧酸代谢及丙酮酸代谢等宿主能量代谢密切相关[31]。肠道微生物群可能通过短链脂肪酸如丁酸盐影响神经元线粒体功能,异常的线粒体功能与不利的细胞稳态相结合可能是肠道微生物群影响抑郁症进展的关键介质[32]。焦虑抑郁症患者肠黏膜屏障通透性增高的血浆标志物连带蛋白和肠型脂肪酸结合蛋白(intestinal fatty acid binding protein,FABP2)与血浆内毒素及肠道微生物组改变相关[33]。
郑方等研究表明,慢性轻度不可预知应激造成小鼠肠道菌群结构发生明显改变,菌群多样性、丰度明显下降,表明抑郁和肠道菌群改变密切相关[34]。最近,在慢性可变性应激诱导的抑郁症大鼠模型中使用超高效液相色谱-质谱进行临床前研究的结果表明,与对照相比,在门和属的水平上存在微生物群差异;此外,应激诱导组中氨基酸和脂肪酸水平较低,胆汁酸、次黄嘌呤和甾醇-胆碱含量较高[35]。肠道微生物可通过调节肠黏膜上皮细胞功能影响神经递质的生成[36]。酪酸梭菌对慢性不可预测轻度应激诱导抑郁样行为小鼠的抗抑郁作用部分归因于肠胰高血糖素样肽-1分泌的刺激和脑胰高血糖素样肽-1受体的活化[37]。抑郁大鼠模型粪便代谢组和粪便微生物群的分析表明,几种氨基酸水平发生了变化,包括L-苏氨酸、异亮氨酸、丙氨酸、丝氨酸、酪氨酸和氧化脯氨酸,并且观察到这些氨基酸改变与粪便微生物群之间存在着显著相关性[38]。使用粪便微生物群移植建立了抑郁症的小鼠模型,对模型小鼠不同部分代谢物的联合分析表明:氨酰-tRNA生物合成显著改变,粪便中的代谢物与肝脏关系最密切;“抑郁微生物”可能导致肝脏中的葡萄糖紊乱;由于大脑消耗体内总葡萄糖的25%,肝脏葡萄糖的减少可能导致抑郁行为,这些发现可能有助于确定抑郁症的生物学机制,并提供有关“抑郁症微生物”影响肝脏代谢的证据[39]。肠道微生物在抑郁症发生机制中扮演了重要的角色,但其确切机制仍然不清楚,需要进一步研究。
5、益生菌与抑郁症
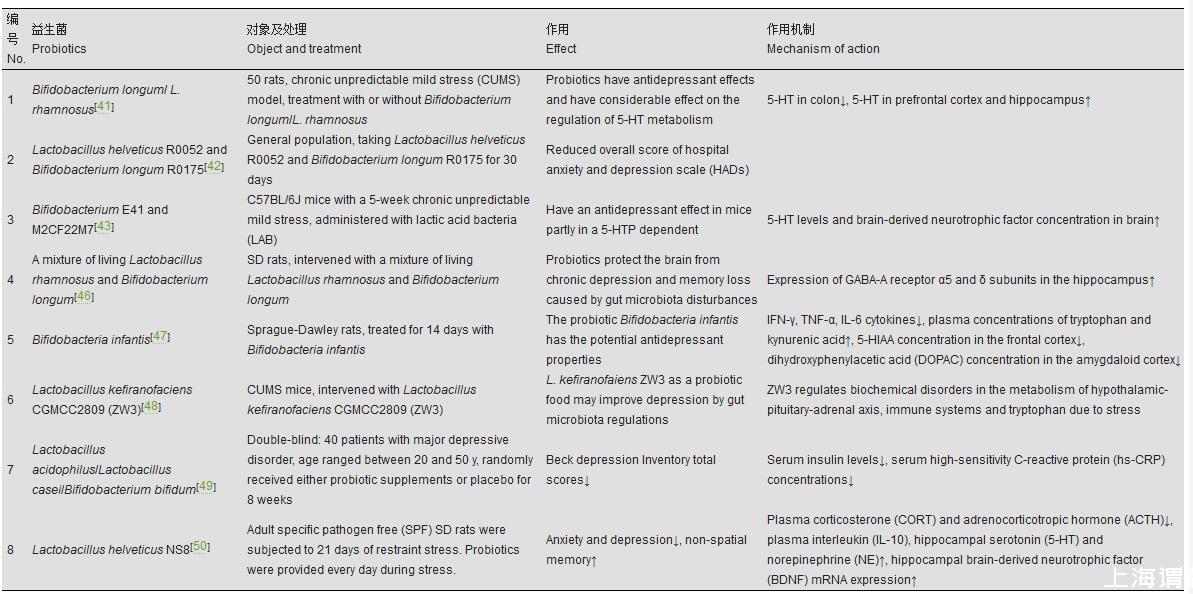
益生菌是一类对宿主有益的活性微生物,传统益生菌主要来自双歧杆菌属(Bifidobacterium)、乳杆菌属(Lactobacillus)和其他一些乳酸菌(lactic acid bacteria,LAB)或酵母菌(yeast)等,补充益生菌可以改变肠道菌群的构成和功能[40]。虽然肠道微生物群与抑郁之间存在复杂关系,但可以通过益生菌调节来改善抑郁症状;表1列出了不同种类益生菌对抑郁症状的改善情况。有研究表明,益生元和益生菌具有抗抑郁作用,对血清素(5-hydoxytryptamine,5-HT)代谢的调节具有相当大的作用,尤其是鼠李糖乳杆菌[41]。在普通人群中证明,瑞士乳杆菌R0052和长双歧杆菌R0175联合服用30 d,可以减少医院焦虑和抑郁量表的整体评分[42]。有研究证明了E41和M2CF22M7可以通过调节五羟基色氨酸(5-hydroxytryptophan,5-HTP)合成来获得抗抑郁作用[43]。益生菌与抑郁症的显著减少相关,非抑郁症患者可以通过接受口服益生菌来降低患抑郁症的风险[44]。补充益生菌能改善抑郁大鼠的情绪状态,影响各种生化指标及脑单胺类神经递质等[45]。研究结果表明:幼年肠道微生物群紊乱可诱导慢性抑郁和记忆丧失,并降低成年大鼠海马中GABA-A受体α5和δ亚基的表达;此外,与短期苯二氮卓类药物治疗相比,适度益生菌给药可显著改善抑郁、记忆症状[46]。益生菌双歧杆菌处理Sprague-Dawley(SD)大鼠14 d后,血清干扰素-γ(serum interferon-γ,IFN-γ)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)和白介素-6(interleukin-6,IL-6)细胞因子显著减弱;此外,与对照组相比,双歧杆菌处理的SD大鼠中,色氨酸和犬尿喹啉酸的血浆浓度显著增加;双歧杆菌处理还导致额叶皮质中5-羟吲哚乙酸(5-hydroxyindole acetic acid,5-HIAA)浓度降低[47]。乳酸杆菌ZW3可调节肠道微生物群的组成,可能通过调节肠道微生物群作为益生菌食物来改善抑郁[48]。一项双盲试验表明,服用益生菌补充剂的患者贝克抑郁量表总分显著降低[49]。有研究表明瑞士乳杆菌NS8对慢性束缚应激抑郁大鼠具有抗抑郁作用[50]。有更多证据表明可以使用益生菌治疗焦虑和抑郁,但与精神科药物相比,任何形式的益生菌都不能被认为是对焦虑和抑郁的可靠治疗。此外,性别差异以及肥胖、生活方式、烟草和酒精使用等合并症可能会影响益生菌的总体益处[51]。补充益生菌可减少重度抑郁症中常见的炎症反应,是一种很有前景的辅助治疗抑郁症方法[52]。益生菌治疗抑郁症的效果有待进一步的临床试验和实验研究验证,具体作用机制还需要进一步阐明。肠道益生菌可以代谢中药有效成分,中药有效成分对肠道益生菌具有调节作用[53],而从中药有效成分角度探讨益生菌与抑郁症之间相互作用的研究仍较少,是将来研究的一个重要方向。
表1益生菌改善抑郁症状
6、中医药与肠道微生物
6.1、中医药与肠道微生态
中医理论包涵了大量与微生态学相关的内容,贯穿在中医“理、法、方、药”的辨证论、治理论体系中。我国微生态学创始人魏曦教授在谈到中医药与微生态时提出,微生态学很可能成为打开中医奥妙大门的一把钥匙[54]。之后,一大批中医药学者积极致力于中医药与肠道微生态的相关研究,并取得了一系列科研成果。肠道微生物的相关理论和中医相关理论在疾病的致病机理和治病原则方面具有高度的统一性,肠道微生物的相关理论也体现了中医整体观、系统观、平衡观和中土思想,传统中医思想的科学内涵可通过现代肠道微生态理论得以部分解析和揭示[55]。通过中医藏象学说、体质学说、正邪致病学说等理论,可以在一定程度上来解释肠道微生态和宿主之间的关系[56]。程成等从中医阴阳学说、中医正邪理论、中医脾胃学说与肠道微生态学的内在联系方面进行了较为详尽的阐述[57]。李晓红等认为,肝主疏泄、调畅情志功能通过调节脑-肠轴上多种神经递质、神经肽、激素及免疫因子的变化而使机体内环境维持稳定[58]。赵雯红等从人体微生态学角度诠释了浊毒理论,是对现代微生物生态学与中医学理论相结合的一个初步尝试[59]。李艳等从中医学“心与小肠相表里”理论角度阐释了中枢神经系统与肠道菌群的关系[60]。姜婷等基于肠道菌群分析了叶天士提出的中医学“上下交损,当治其中”治法的理论依据,并探讨了在慢性、多系统、复杂疾病防治中调节肠道菌群的重要性[61]。肠道菌群、肠道菌群失调与中医“脾胃”“脾胃之气”“脾胃功能失调”密切关联,高丽娟等分析了中医“脾胃”与肠道微生物群的关系,并从“微生物-肠-脑轴”理论角度进一步探讨“脾胃为后天之本”[62]。总之,肠道微生物的相关理论和中医相关理论在疾病病理生理、治疗预防等方面具有高度的统一性,两种理论的异同之处有待进一步挖掘与阐释。
同一证型的肠道菌群结构可因病种、病位、病机不同而出现差异,肠道微生态与中医证候的变化规律可能是同病异治与异病同治的重要依据,而将肠道微生态融入到中医证候的研究,可以深化对中医证候内涵的新认识[63]。研究表明,不同中医证型的溃疡性结肠炎患者肠道菌群的构成及菌群代谢特征差异明显,其中副拟杆菌属含量下降与肝郁脾虚证相关性高,有潜力成为诊断肝郁脾虚证溃疡性结肠炎的诊断性生物标记物[64]。肝阳上亢型急性脑出血与肠道菌群结构紊乱有关,其中普氏菌和阿克曼粘细菌的相对丰度下降是其发生的主要原因,补充和调节阿克曼粘细菌、普氏菌的丰度值可能是靶向治疗和预防急性脑出血的有效途径之一[65]。帕金森具有多种肠道菌群寄生,拟杆菌门与中医内热证相关,而非特异的厚壁菌门分别与内热证和痰浊证负相关,其对中医药选择治疗具有潜在指导价值[66]。中焦湿热证所属的胃肠道相关疾病会出现肠道菌群失衡的情况,表现为益生菌大量减少,有害菌大量增加,说明胃肠道菌群失衡、菌群发生易位可能是中焦湿热证和胃肠道微生态紊乱所属疾病的共同发病基础[67]。
中药复方不仅可通过活性物质作用于靶器官发挥作用,还可以调整肠道菌群治疗疾病,具有多成分、多层次、多靶点起效的特点,而纠正肠道微生态紊乱也已经成为中医药防治疾病的重要治疗策略。中医方剂在疾病临床疗效发挥方面扮演了重要角色,方剂有效成分及其代谢产物通过胃肠道吸收入血发挥疗效,而肠道中未吸收的成分通过调控肠道菌群也能发挥疾病治疗作用[68]。研究表明痛泻要方不但能够使肝气乘脾泄泻小鼠肠道内容物中微生物活度降低,恢复至正常水平,还能增加肠黏膜中段、后段微生物活度[69]。痛泻要方对肝郁脾虚型肠易激综合征的临床研究表明,痛泻要方组患者治疗后肠道嗜酸乳杆菌、双歧杆菌、粪链球菌数量明显增加,与对照组比较差异明显,说明痛泻要方可调节肠道菌群丰度,增加肠道有益菌数量[70]。越鞠丸可能通过抑制红蝽菌科、普雷沃氏菌科、S24-7科、气单胞菌科细菌和促进双歧杆菌科、理研菌科、乳杆菌科、毛螺菌科、产氢细菌目细菌的生长起到降低甘油三酯和低密度脂蛋白的作用[71]。吴秀等的研究中脾虚小鼠肠道双歧杆菌、乳酸杆菌、脆弱拟杆菌和大肠杆菌数量明显增多,双歧杆菌与大肠杆菌的定殖抗力之比(Bifidobacterium/Enterobacillus,B/E)降低,经四君子多糖治疗后,菌落数及B/E值趋于恢复正常[72]。
七味白术散能纠正肠道菌群失调小鼠的腹泻,其机制可能在于促进受损肠黏膜损伤修复和减少炎症细胞因子的释放[73]。益气化痰祛瘀方能影响肠道微生物种类、组成和丰度,调控短链脂肪酸的生成可能是其治疗阻塞性睡眠呼吸暂停低通气综合征肝损伤的机制之一[74]。吴国琳等通过整理中药复方调整肠道菌群研究的相关文献,总结得出具有健脾益气、通便理气、化湿止泻、清热解毒、消食化积等作用的中药复方对肠道微生态具有调节作用[75]。中医证候客观化的研究是目前中医基础和临床研究的重点和难点,肠道菌群的相关研究可能会给中医辨证提供一些客观化证据[76],而目前关于肠道微生态与中医证候相关性的研究主要集中在脾虚证与肠道菌群的变化关系及健脾方剂对肠道微生态多样性和菌群组成的影响[77]。当然,证候的肠道菌群机制研究现在还处于初步研究阶段,有必要进一步探讨更多的中药复方对相关病证的治疗效果与机制来更好地指导临床实践。
调控肠道微生物稳态是中药起效方式的重要补充,聚类分析显示,治疗肠道菌群失调的中药主要以补气健脾、渗湿利水类为常见[63]。健脾中药含有多糖类、黄酮类、生物碱类等多种生物活性成分,可以从扶植有益菌生长、调节肠道运动、抑制炎症因子、保护肠道黏膜等不同的途径对疾病发挥治疗作用[78]。中药调节肠道菌群治疗脑血管疾病,主要表现在重塑肠道微环境、增加益生菌、减弱菌群易位,以改善脑血管损伤[79]。高通量测序技术研究蚕沙对湿阻中焦证大鼠肠道菌群的影响提示,蚕沙可能通过平衡肠道菌群发挥治疗湿阻中焦的作用,而这种作用可能与蚕沙药材中微生物的代谢产物有关[80]。黄连提取物可明显促进益生菌(乳酸菌、双歧杆菌)的生长,显著抑制病原菌的生长,而且调控作用与剂量呈正相关性[81]。另外,鲜品中药所含有的活性内生菌也可能通过被摄入的方式直接参与肠道菌群的调控,我们对中药有效成分皂苷对肠道微生态的调节作用及免疫机制研究进行了总结,为中药有效成分对肠道微生态的免疫调节作用及机制研究提供了理论依据[82]。另外,丁佳敏等提出了“中药肠中移行成分”等概念,认为肠中移行成分是方剂发挥疾病治疗作用的重要物质基础[68]。中药及中药复方成分复杂,明确其具体调节肠道微生态结构和功能的物质基础等问题,有待于进一步阐释,仍需我们继续努力。
通过菌群移植重建肠道内的正常微环境,可以有效地治疗脑肠相关疾病[83]。在《伤寒论》和《内经》等中医经典中就有关于脑肠相互联系的描述[84]。葛洪在《肘后备急方》中记载“并善,又绞粪汁,饮数合至一二升,谓之黄龙汤,陈久者佳”来治疗腹部严重泄泻和食物中毒,这体现了中医药使用粪菌移植来治疗疾病的方法[77]。中医可用金汁等粪便类药物调控肠道菌群,众多疾病正在尝试应用粪便移植来进行治疗[85]。粪便类中药与粪菌移植均为应用粪便治疗疾病的有效方法,临床常用的粪便有白丁香、蚕沙、鸡矢白、金汁、两头尖、龙涎香、人中黄、望月砂、五灵脂等[86]。马艳苗等从“阳明”的概念、所属脏腑经络入手,解析了《伤寒论》阳明病篇中通下法运用对神志状态的影响,探讨了脑肠相关与中医通下的关系[87]。总之,通过使用粪便类中药和菌群移植治疗疾病,给我们治疗疾病提供了新视角,而通过粪便移植探究中药及中药复方对疾病、症状的改善作用有待于进一步研究。
6.2、中医药与抑郁症肠道微生态
大量的临床及动物实验研究表明,中医药有助于调节、恢复紊乱的肠道菌群,而中医药在抑郁症肠道菌群理论探索方面,张晓梅等提出肠道菌群代谢物质可能是肠道微环境与神明密切相关的物质基础,神经系统可能是肠道微环境与神明密切相关的网络系统[88]。抑郁症中医肠道菌群机制研究表明,肝主疏泄和调畅情志功能通过调节脑-肠轴上多种神经递质、神经肽、激素及免疫因子的变化而使机体内环境维持稳定[58]。色氨酸是5-HT的前体,色氨酸缺乏可以诱导大鼠抑郁样行为;另外,犬尿氨酸在抑郁症患者中上调,天丝饮(巴戟天和菟丝子)通过调节色氨酸-犬尿氨酸途径中的肠道微生物群组成和代谢物来改善大鼠的抑郁症状[89]。加味逍遥颗粒辅助治疗肝郁脾虚证抑郁症4周后,肠杆菌低于对照组,乳酸杆菌、双歧杆菌及B/E比值高于对照组,差异有统计学意义,说明加味逍遥颗粒可改善肠道菌群,这可能是加味逍遥颗粒组抑郁症状改善更明显的原因之一[90]。逍遥散煎剂调节了拟杆菌、变形杆菌、厚壁菌、绿弯菌和浮霉菌的丰度;在属的水平上,逍遥散煎剂减少了普雷沃菌和脱硫弧菌的丰度,增加了瘤胃球菌家族的丰度,以改善抑郁样行为;该过程涉及的机制可能与短链脂肪酸,脂多糖和肠道炎症有关[91]。逍遥散低极性部位给药可以增加慢性不可预知温和应激(chronic unpredictable mild stress,CUMS)模型大鼠微生物群的多样性,显著回调CUMS模型大鼠肠道微生物中罗斯氏菌属和普雷沃氏菌属,它们主要与肠道炎症和短链脂肪酸的产生有关[92]。颐脑解郁复方通过增加卒中后应激大鼠肠道中乳杆菌属和拟杆菌属的数量,从而减轻了其抑郁症状[93]。
管花肉苁蓉可调节慢性不可预知刺激致抑郁大鼠紊乱的肠道菌群及肠道菌群代谢产物短链脂肪酸的产生,恢复肠道菌群结构稳态[94]。从中药黄连中分离的小檗碱可逆转胃粘膜内的应激和胃、回肠、盲肠和结肠的肠道微绒毛所带来的物理损伤,高浓度的小檗碱可显著保护大鼠免受慢性压力和抑郁症的各种症状[95]。白藜芦醇通过调节脑-肠轴中的5-HT1A依赖性蛋白激酶A-环磷酸腺苷反应元件结合蛋白-脑源性神经营养因子(protein kinase A-cyclic adenosine monophosphate response element binding protein-brain derived neurotrophic factor,PKA-CREB-BDNF)信号传导,改善了肠易激综合征大鼠模型中应激相关抑郁、焦虑症状[96]。芍药苷具有显著的抗抑郁活性,其通过肠道微生物群转化为苯甲酸,主要通过尿液排泄,肠道代谢产物苯甲酸作为主要的排泄形式;芍药苷还可通过增加益生菌的丰度来调节肠道微生物群的组成;此外,芍药苷可通过肠道微生物群代谢成苯甲酸,这可能通过血脑屏障向大脑发挥抗抑郁作用[97]。总之,肠道菌群可能是中医药治疗抑郁症的新靶点,中医药可能通过肠道菌群来起到抗抑郁作用。
另外,针灸对肠道菌群也具有调节作用,并且这种调节作用有可能是通过对脑肠轴的调节实现的[98]。针灸可以通过调理气机升降调节肠道微生物群;针灸可以调节肠道微生物群的数量和比例,使其恢复稳态;针灸还可以通过调控脑肠肽、炎性反应调节肠道微生物群[99]。有研究表明,针灸可以提高肠道细菌的丰富度及多样性、增加某些益生菌的含量[100]。也有研究表明,音乐电针、脉冲电针和氟西汀对抑郁模型大鼠肠道菌群每孔颜色平均变化率值表达有调节作用[101]。目前,针灸对抑郁症肠道菌群的研究还较少,因此,今后应深入探究肠道菌群在治疗抑郁症患者中的作用以及针灸对其具体的调控机制,这将为针灸治疗抑郁症的机制提供新的思路和研究途径。
7、小结
对于各种躯体和精神疾病,人类微生物群与其宿主相互作用的研究正在迅速增加[102],人类肠道微生物科、属、种的分子和生物化学完整性与维持外周器官系统和中枢神经系统神经元群的复杂代谢和行为过程密切相关[103]。从众多候选差异菌群中筛选出抑郁相关的关键菌株仍充满挑战。微生物组研究正成为新一轮科技浪潮的前沿阵地,目前中国科学院微生物组计划已经启动,而探讨中医药药效与抑郁症等肠道微生物组的因果关系,对于发展基于微生物组的抑郁症中医药治疗和预防,阐释中医药的脑肠理论等都具有重要的意义。尽管指纹图谱技术、宏基因组学技术、微生物组学、蛋白组学、代谢组学、生物信息学等新技术方法的应用,将扩展我们对微生物群组分与宿主之间相互作用的复杂作用机制的认识[104],但肠道是一个复杂的生态系统,临床研究肠道微生物群的组成和功能受到遗传、年龄、性别、饮食、区域、精神和身体疾病等多种因素的影响,研究也会面临许多限制和不足。大多数临床研究中的招募受试者没有接受标准化饮食,并且地理影响也没有受到严格控制[105]。因此,在将来的临床研究中,应尽量建立统一的标准,考虑肠道菌群微生物特征与相关影响因素,结合中医药理论,对相关结果进行合理的阐释。
利用机器学习方法,基于肠道菌群的扩增子序列变异对肠道菌群的分类群及功能进行分析,可显著区分出具有抑郁表型的个体,或可用于辅助抑郁症的诊断与鉴别,这为中医基于肠道菌群的客观化辨证研究提供了新的启示[106]。选择性5-羟色胺再摄取抑制剂(selective serotonin reuptake inhibitor,SSRI)能够改变肠道微生物群,药物对肠道微生物组分的影响也越来越明显[107]。同时,临床前研究已经描绘出肠道微生物在不同脑区的结构和活动水平上的影响[108]。微生态药物在许多复杂性和慢性疾病中显示出极大的潜力,逐渐成为国际制药行业的新趋势。全球共有142个在研微生态药物,其中49个药物处于临床阶段[109]。中药复方是中医药理论的具体体现,由于中药复方组方的复杂性及有效成分的复杂性,这给体内成分的检测和生物活性成分研究带来了很大困难。因此,生物活性成分的研究是中医药亟待阐明的问题,未来中医药的研究,需要关注中药复方中的哪些成分起到了调节肠道菌群的效果,并根据生物活性成分的属性或可能的靶点进行分类研究,进而深入研究各种成分的配比或者协同作用。
许多研究证明,中医复方、单味中药、中药有效成分、针灸等通过肠道微生物对抑郁症有调节作用,但仍需进一步梳理和研究中医学所包涵的微生态内容,继续探讨、验证中医药微生态的理论与应用。随着微生物-肠-脑轴与抑郁症关系的探讨,将有助于对抑郁症发病机制的认识,而研究中医药对抑郁症肠道微生物的作用,为临床预防和治疗抑郁症提供了新的研究思路和方法。我们认为,中医对抑郁症的治疗需注重调整“脑神-心神-五脏神”协调相衡。抑郁症的治疗应以气血为纲、联络脏腑,旨在调节脑神,并提出“脑神-心神-五脏神-情志活动-躯体症状和/或生物学症状”理论,针对抑郁症是脑窍郁闭、元神被扼、肝失疏泄、心神不安、脾失运化、脏腑气血阴阳失调、神机不运之中医病机,拟定了以疏肝解郁、养心安神为主要治则的经验方——解郁胶囊,在疏肝解郁治则的基础上,重视丹参、岷当归等调养气血、养心安神药物的应用[110]。临床研究方面,本课题组正在对抑郁症患者粪便进行16S rRNA基因测序,分析抑郁症患者肠道菌群特点,并分析西药帕罗西汀及中药“解郁胶囊”对肠道菌群的影响,探讨解郁胶囊治疗抑郁症可能的作用及肠道菌群作用机制。在动物实验方面,本课题组正基于Wingless/Integrated(Wnt)信号通路,探讨“解郁胶囊”通过肠道菌群对抑郁大鼠的调节作用及作用机制,为中医药通过微生态调节机制治疗抑郁症提供理论依据。目前,影响焦虑和抑郁相关行为的特定细菌仍不清楚,抑郁症客观诊断学标记和靶向治疗等重要临床问题仍知之甚少。因此,基于“微生物-肠-脑轴”理论,寻找高灵敏度和高特异性的抑郁症诊断和评估的肠道微生物,是我们探索的重要目标之一。然而将传统中医学与肠道微生物学相结合,以中医理论为指导,以临床实践为基础,为抑郁症证候找到客观、微观、动态的微生物学基础,为辨证提供客观化、规范化的新指标,为深入研究和认识中医学“理、法、方、药”的科学内涵提供更多、更有价值的证据,将是我们未来研究的重要方向。
 相关新闻
相关新闻