热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
2.2 Fe-CDs的光谱性质
通过紫外可见吸收光谱仪和荧光光谱仪表征Fe-CDs的光谱性能。如图4(a)所示,在紫外可见吸收光谱中Fe-CDs在300 nm和425 nm附近表现出明显的宽吸收峰,分别归因于Fe-CDs内核共轭体系的π→π*跃迁,及表面多种官能团的n→π*跃迁。从荧光光谱可以看出Fe-CDs的最佳激发和发射波长分别为449 nm和571 nm。Fe-CDs在紫外灯照射下可以看到明亮的黄色荧光。从不同激发波长下Fe-CDs的发射光谱数据(图4b)可以看到,当激发波长由390 nm增加到550 nm时,Fe-CDs的荧光发射波长几乎没有明显的变化,荧光强度先增加后下降,表明Fe-CDs的发光性质是激发波长独立性的,这可能是由于Fe-CDs的粒径及发射中心相对均匀的原因。另外,相较于其他金属掺杂碳点,Fe-CDs表现出高的荧光量子产率,以罗丹明6G(乙醇中QY=95%)为参照,其量子产率可达26.80%(表1)。
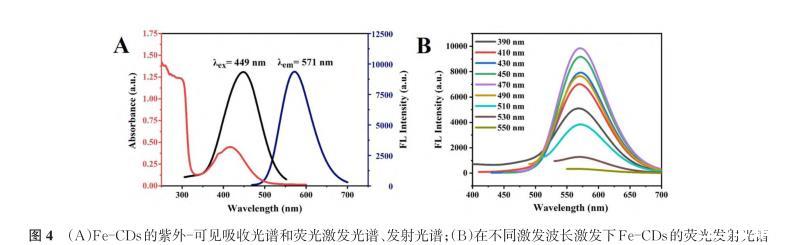
图4(a)Fe-CDs的紫外-可见吸收光谱和荧光激发光谱、发射光谱;(b)在不同激发波长激发下Fe-CDs的荧光发射光谱
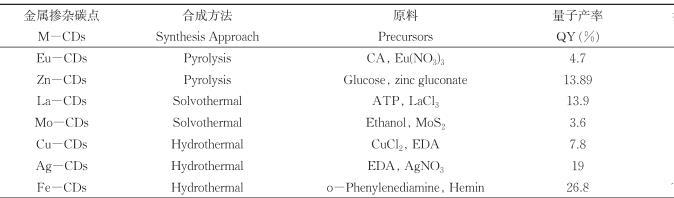
表1不同金属掺杂碳点的荧光量子产率对比
为了研究Fe-CDs的荧光稳定性,考察了不同离子强度、金属离子及氨基酸对Fe-CDs荧光强度的影响。如图5(a),以不同浓度NaCl溶液模拟不同离子强度环境,当NaCl溶液浓度高达到2.0 mol/L时,荧光强度依然可维持原始荧光强度的90%以上,表明Fe-CDs具有良好的离子稳定性和抗盐能力。如图5(b)和5(c)所示,当Fe-CDs分别与15种不同的金属离子及17种不同的氨基酸共存时,Fe-CDs荧光强度几乎不受各种共存物质的影响,表明Fe-CDs有比较强的光稳定性。

图5(a)不同浓度的盐溶液对Fe-CDs荧光强度的影响;(b)不同金属离子对Fe-CDs荧光强度的影响;(c)不同氨基酸对Fe-CDs荧光强度的影响
2.3 Fe-CDs荧光探针检测pH
pH在很大程度上影响着机体的正常功能,开发用于监测细胞内pH变化的新型荧光探针对于研究pH影响的相关的疾病具有重要意义。由于Fe-CDs表面存在丰富的活性官能团,我们探索了其在传感器领域的潜在应用。如图6(a)所示,Fe-CDs在酸性环境下的荧光强度随着pH的减小逐渐降低(λex=449 nm,λem=571 nm)。当pH降低至2时,Fe-CDs 95%的荧光强度被猝灭;当pH为7时Fe-CDs荧光强度达到最高值。在碱性环境下,随着pH的逐渐增大,Fe-CDs荧光强度变化不大。通过玻尔兹曼函数拟合曲线,得到Fe-CDs的pKa为5.32,且在pH 4.4~6.2范围内,Fe-CDs荧光强度与pH具有良好的线性相关性,y=4086 pH-16 800.5(图6b)。上述实验结果证明Fe-CDs可作为监测酸性条件下pH变化的新型荧光探针。
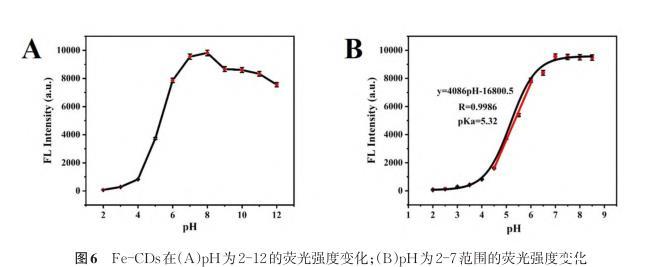
图6 Fe-CDs随pH值的荧光强度变化(a)pH为2~12的荧光强度变化;(b)pH为2~7范围的荧光强度变化
通过检测不同pH下的Fe-CDs的Zeta电位、荧光寿命及紫外吸收光谱,研究了Fe-CDs检测pH的作用机理。由Zeta电位结果可知,pH从7降至2时,随着体系中H+浓度的升高Fe-CDs的所带电荷由-9.39 mV升高至16.6 mV。同时Fe-CDs的荧光寿命由1.70 ns升高至2.23 ns(图7a)。从紫外吸收光谱可知,随着pH的逐渐减小,Fe-CDs在425 nm处的吸收峰逐渐红移至450 nm(图7b)。因此,推测Fe-CDs表现出pH依赖的荧光特性可能是由于pH值的变化导致Fe-CDs中π→π*和n→π*电子跃迁变化引起的,Fe-CDs表面的羧基、氨基等官能团的质子化和解质子化造成其费米能级的偏移使其表现出pH依赖的荧光特性。
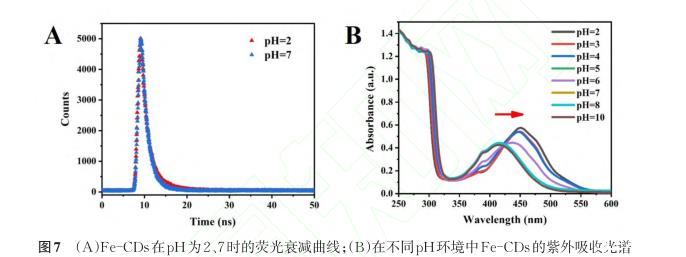
图7(a)Fe-CDs在pH为2、7时的荧光衰减曲线;(b)在不同pH环境中Fe-CDs的紫外吸收光谱
2.4 Fe-CDs的细胞毒性及其在细胞成像中的应用
通过上述研究证明,Fe-CDs可作为监测酸性条件下pH变化的新型荧光探针,在成像应用中具有发展潜力。首先,我们选用人宫颈癌HeLa细胞为模型,采用MTT标准法检测Fe-CDs的细胞毒性。如图8中所示,用不同浓度的Fe-CDs与HeLa细胞共孵育24 h后,即使Fe-CDs的浓度达到300μg/mL,HeLa细胞的存活率仍高于85%,说明Fe-CDs毒性非常低,具有良好的生物相容性,可有效应用于体内细胞成像。
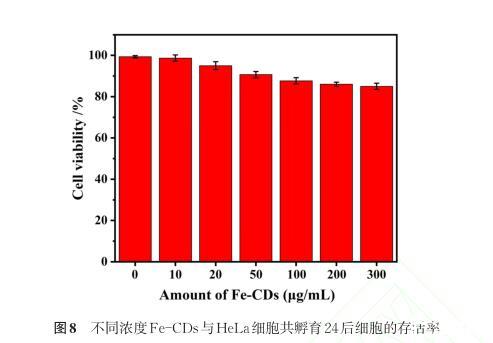
图8不同浓度Fe-CDs与HeLa细胞共孵育24 h后细胞的存活率
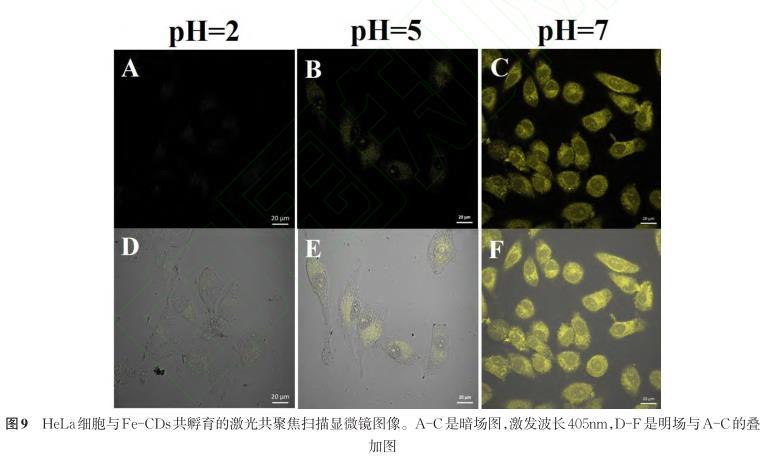
由于Fe-CDs具有良好的光学性能及稳定的生物相容性,探索了其作为荧光探针在监测细胞内pH的可能性。用人宫颈癌HeLa细胞为模型,将浓度为0.1 mg/mL的不同pH值的(pH=2,5,7)Fe-CDs与HeLa细胞共孵育半小时进行细胞成像实验,观察细胞形态变化以及细胞内荧光变化。如图9所示,Fe-CDs分布于细胞膜、细胞质甚至细胞核区域,说明Fe-CDs具有良好的细胞通透性。当pH为7时,细胞内的荧光强度最强(c和f);当pH为5时,Fe-CDs的荧光强度部分猝灭(b和e);当pH为2时,Fe-CDs的荧光强度几乎全部被猝灭(a和d)。这与体外实验结果一致,也进一步表明了Fe-CDs可作为一种良好的pH荧光探针用于细胞内pH水平的监测。
3结论
该工作以邻苯二胺及生物分子血红素为原料,通过一步水热法制备得到铁掺杂荧光碳点(Fe-CDs)。由于原料中的血红素具有大环结构,利于碳点在合成过程形成大的共轭平面;并且微量的铁元素掺杂有助于改变碳点的电荷分布,进而大幅提高了碳点的荧光量子产率,可达26.8%。同时,Fe-CDs展现出良好的水溶性,稳定的光学性能,优异的抗盐及抗干扰能力。由于其表面丰富的氨基、羧基等官能团及铁元素的掺杂,Fe-CDs可以作为荧光探针用于酸性环境下的pH检测。同时Fe-CDs具有低毒性且易于被细胞摄取,可实现细胞内pH的荧光成像应用。以上研究证明Fe-CDs作为一种制备简便、性能优异的荧光探针在生物传感领域具有良好的应用潜力。
 相关新闻
相关新闻