热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
心脏骤停(cardiac arrest,CA)是指各种原因导致的心脏射血功能突然停止,是临床上常见的急危重症之一。心脏骤停已成为危害现代人健康与生存的严重性疾患。如何提高心肺复苏成功率,探索心肺脑复苏过程中血液断流、缺血缺氧对心肌代谢和多器官功能的影响,减少PR-MODS的形成,探索治疗中的干预措施和药物应用方法。目前仍主要依靠动物模型的建立,然而如何成功复制出与人类心脏骤停心肺复苏病理生理学改变过程相似的动物模型,获得有临床实用价值的研究成果,一直都是心肺脑复苏领域研究的难点和焦点问题。本论文使用了老鼠模型进行研究,观察老鼠直接脑缺血和大鼠窒息性心跳停止后对老鼠大脑皮层和丘脑中的氧气浓度进行监测。
微电极的应用
老鼠大脑的固定是使用释义立式定位仪用耳棒,老鼠脑部的氧气浓度的在线监测是使用克拉克型氧微电极(Ox-50,Unisense,Denmark)中。老鼠大脑皮层的氧气浓度(O2)是使用微电极插入大脑皮层深度为1 mm,而老鼠丘脑部分氧分压浓度使用微电极插入到老鼠大脑内深度为6mm。
实验结果
老鼠大脑皮层区域以及丘脑区域具有类似的氧分压基线(PbO2),这些区域都表现为早期的持续缺氧状态。通过对比发现,老鼠丘脑区域的氧分压值表现为先增加到4倍的起始值后降低到起始的基线值。当对老鼠进行心脏骤停导致其窒息后,老鼠脑部区域的脑氧合出现差异变化,首先是大脑皮层区域出现,接着是丘脑组织氧过多,这种大脑皮层区域氧分压值的测试代表了一种作为在临床中实现对心脏骤停中后神经功能恢复病例的治疗方法。
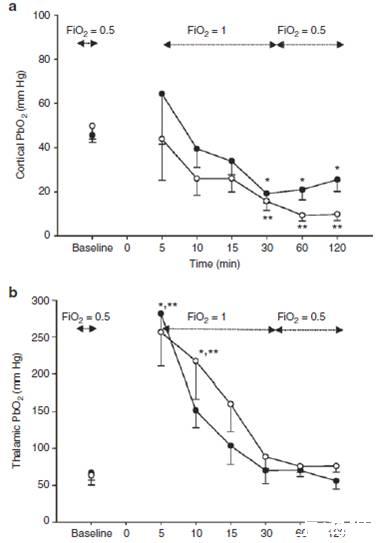
图1、心脏骤停的老鼠进行心脏复苏后老鼠大脑氧分压变化情况。图a表示的是老鼠大脑皮层区域的氧分压值、图b指的是老鼠丘脑区域的氧分压值变化情况。其中横坐标的零表示的是老鼠心脏开始骤停开始。黑色圆圈表示是心脏骤停9分钟的实验老鼠,空心圆圈表示的是心脏骤停12分钟的实验老鼠。从图中可以看出,当实验的老鼠心脏骤停的时间越长,老鼠大脑皮层区域的脑部氧分压浓度越低,而在老鼠丘脑区域则相反,即老鼠心脏骤停的时间越短,其老鼠丘脑区域的脑部氧分压浓度越低,并且随着时间的增加,其老鼠脑部的氧分压浓度会逐渐的降低。
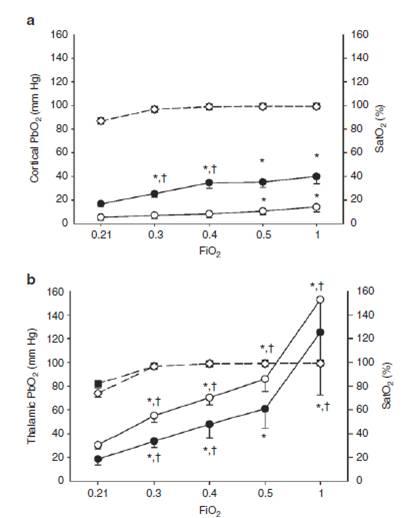
图2、心脏骤停(CA)后老鼠的脑组织氧分压及动脉血氧饱和度(a)大脑皮层区域(b)丘脑区域。其中黑色圆圈表示的是心脏骤停9分钟的实验室老鼠的脑组织氧分压(Pb O2);空气圆圈表示的是心脏骤停12分钟的实验室老鼠的脑组织氧分压(Pb O2),黑色菱形代表了心脏骤停12分钟的实验室老鼠的动脉血氧饱和度。每批次试验的老鼠是六只为一组。从图中可以看出,心脏骤停(CA)后老鼠大脑皮层的脑组织氧分压在10-40 mmHg之间,而老鼠丘脑的脑组织氧分压在20-140 mmHg之间变化。
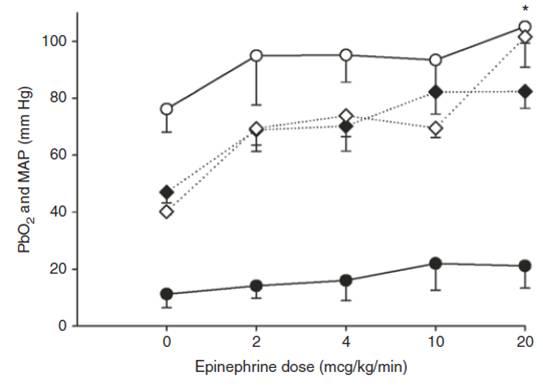
图3、心脏骤停(12分钟的窒息)老鼠复苏后120分钟,老鼠体内肾上腺素注射前和注射后的老鼠大脑皮层的动脉血氧分压以及动脉血压的变化情况。其中黑色圆圈表示的是大脑皮层的氧分压,白色圆圈表示的是老鼠丘脑区域的氧分压,黑色菱形表示的是大脑皮层的动脉血压的变化情况,白色菱形表示的是老鼠丘脑区域的动脉血氧的变化情况。每批次的实验老鼠是6只。从图中可以看出,随着肾上腺素注射浓度增加,老鼠的脑组织氧分压以及动脉血压逐渐增加。
总结
心脏骤停已成为危害现代人健康与生存的严重性疾患。心脏骤停动物模型在研究人类心肺复苏技术、探讨心脏骤停前后病理生理学及分子生物学发生机制、研究复苏药物及其它干预治疗手段等多方面都具有非常重要的意义。本论文以老鼠为动物模型进行研究,研究其心脏骤停的不同发生机制,探索老鼠心脏骤停(CA)后脑氧分压值的变化情况以及再复苏时老鼠的大脑氧分压值的变化情况,论文中所有氧分压的测试是应用了unisense微电极系统中氧气微电极对老鼠大脑不同区域氧分压值进行活体的原位检测,这也说明unisense系统在动物心肺脑复苏领域的研究方向存在着很好的应用前景。
 相关新闻
相关新闻