热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
由于柔性电极在减轻脑组织损伤和信号获取上都展现出了更大的潜力,是科研界和产业界重点投入研发的领域。目前,超柔性和高密度是主攻突破方向。
超柔性
由于脑组织杨氏模量极低(0.4-15kPa),因此电极材料的选取变得尤为关键。硅基材料杨氏模量过高,在中国已经不是主流材料。除了聚酰亚胺、聚对二甲苯等可以微纳加工的聚合物外,弹性硅胶材料和超柔性水凝胶材料也颇受关注。这里的取舍是:材料越软,和脑组织的机械匹配性就越好,精细化微纳加工难度就越大。
在水凝胶方面,2023年,中科院长春应化所张强研究员研发的水凝胶电极通过引入聚轮烷结构作为交联剂,成功实现大鼠脑神经信号长期记录。2022年,西南交通大学的鲁雄教授、谢超鸣副教授团队、电子科技大学潘泰松副教授、中国海洋大学韩璐教授和北京基础医学研究所江小霞副研究员共同研发了具有脑组织力学和生物学匹配性的水凝胶电极,具有免疫逃逸性。
在弹性硅胶材料方面,聚二甲基硅氧烷(PDMS)由于具有极佳的透光性、化学稳定性、热稳定性、生物相容性以及最重要的可加工性而展现出巨大潜力。实操难点上,PDMS材料的图形化工艺尚不成熟且精度有限,同时PDMS有较高的水汽透过率,会对植入体内导电材料造成氧化和腐蚀问题。其加工精度和长期可靠性是下一步研发的重点。
高密度
如之前所说,越柔软的电极带来的问题便是更难的精细化微纳加工。从技术(柔性和加工难度、成本)平衡取舍的角度,提高密度将引入全新的参考变量。
人体大脑约有860亿个神经元,现有脑机接口的通量显然是不足以处理如此巨大的输入。电极通道数量增加会带来一系列如电路连接、神经信号高保真放大滤波、数据算法处理、以及最现实的数据传输供电及散热问题。提高密度为硬件颠覆式迭代之前的可行方向。
国内方面,科研端和产业端都有极具特色的技术路径。
上海阶梯医疗的高通量超柔性微纳电极,可实现最高2304通道的无免疫瘢痕植入,植入300天以上后仍能稳定采集脑电波信号。团队的设计方案是在材料本身柔性的极限内,通过降低电极厚度来降低弯曲应力,从而达到了细胞间作用力的量级,使细胞感知不到电极的存在。
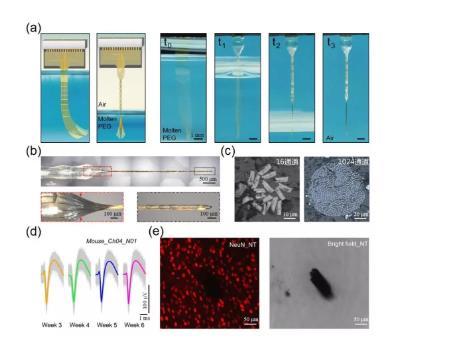
中科院脑科学与智能技术卓越创新中心、国家纳米科学中心方英研究员和神经科学研究所李澄宇研究员及其团队研发了名为“神经流苏”的技术,通过将上千根与神经元突触尺寸接近柔性神经纤维电极浸入在聚乙二醇液体中,利用表面张力聚合“流苏”,待成功植入并降解代谢聚乙二醇后,柔性神经纤维电极自动释放。此方法通过优化植入方式来增加脑内纤维电极的数量。
同样借助创新性植入方法的还有上海脑虎科技。团队利用蚕丝蛋白抗菌、可降解、相容性好、机械性能佳的特点,将其包裹在MEMS集成电路工艺加工的高密度柔性电极外,使其固化,将硬度控制在血管和脑组织之间。植入后,蚕丝蛋白降解并释放柔性电极。目前,该技术仍在实验室阶段并已开展相关专利及产品报审。
随着一批技术逐渐在临床开展推进,其效果将很快在产业端产生波动。