热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
2.3动电位极化曲线分析
图4为黄铜电极在无菌与含菌试验介质中浸泡不同时间的极化曲线。表2为根据极化曲线计算得到的腐蚀电流密度。由表2可见,含菌溶液中电极的腐蚀电流密度要大于无菌溶液中。在无菌溶液中,随着浸泡时间的延长,电极腐蚀电流密度逐渐减小,从浸泡前期(1 d)的0.96μA·cm-2到浸泡后期(14 d)的0.83μA·cm-2,说明黄铜电极的耐蚀性能有所提高;而在含菌体系中,随着浸泡时间的延长,电极腐蚀电流密度从浸泡第1天的1.31μA·cm-2逐渐增大到浸泡第14天的11.04μA·cm-2,说明含菌溶液促进了黄铜电极的腐蚀。极化曲线试验结果与阻抗谱结果相吻合。
一般认为,SRB促进金属腐蚀的原因是由于其参与了腐蚀的阴极过程。首先在缺氧条件下,水发生电离产生去极化剂的H+。

由于金属铜、锌、铁表面的析氢过电位较高,氢气较难析出,H+被还原后在金属表面吸附积累成氢原子层,使阴极反应受到一定程度的抑制。当溶液中存在SRB时,SRB自身存在的氢化酶能够将吸附在电极表面的氢原子层消耗掉,从而促使阴极反应的顺利进行;同时SRB通过生长代谢将SO42-还原成H2S,进而电离成具有腐蚀性的HS-和S2-:
另外微生物在金属表面的附着起到了屏蔽溶解氧的作用,在缺氧的微生物膜下金属部位成为阳极,膜下SRB生成的HS-吸附在黄铜电极表面,使得膜下金属局部pH降低,铜表面电位产生差异,导致黄铜合金中电位较负、活泼性较大的锌组分发生溶解,而在HS-的吸附下,铜也可逐渐氧化为Cu+。
生成的Zn2+直接进入溶液,而由于溶解的Cu2+和Cu+不稳定,会与溶液中的HS-和S2-发生如下反应:
SRB的阴极去极化作用加速了黄铜腐蚀的进行,而当溶解的金属阳离子Cu+与Cu2+与溶液中的HS-和S2-反应生成Cu2S和CuS致密硫化物覆盖在黄铜表面时,又会暂时阻碍黄铜腐蚀反应的进行,这就对应了电化学阻抗谱(图2)和极化曲线(图4)显示的黄铜耐蚀性能先增大、后减小的趋势。

图4黄铜电极在两种介质中浸泡不同时间的极化曲线
2.4丝束电极测试分析
在含菌试验介质中测量丝束电极的单电极腐蚀电位极差(丝束电极中单电极间腐蚀电位的最大差值:E最正-E最负)随时间变化规律以及浸泡1 d与14 d的丝束电极腐蚀电位分布图,如图5与图6所示。
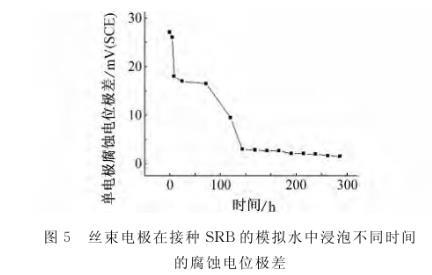
图5丝束电极在接种SRB的模拟水中浸泡不同时间的腐蚀电位极差
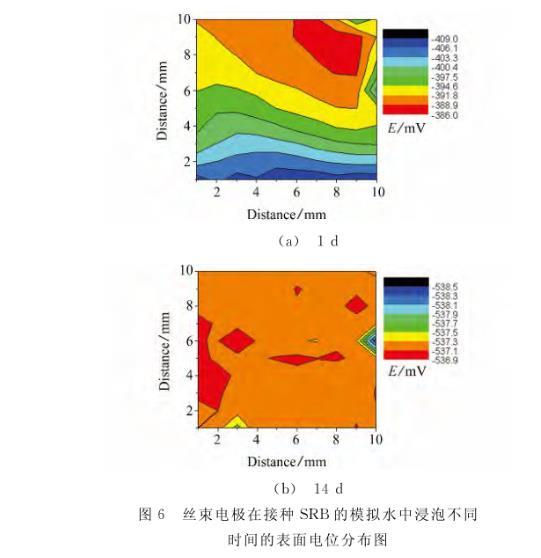
图6丝束电极在接种SRB的模拟水中浸泡不同时间的表面电位分布图
图5表明,丝束电极在含SRB的试验介质中浸泡初期,单电极腐蚀电位极差值较大,最大达到28 mV。从图6(a)可以看出,电极表面的电位分布较不均匀。图5显示,随着浸泡时间的延长,丝束电极单电极间腐蚀电位极差值逐渐减小,150 h后减小到2 mV左右并基本稳定,从图6(b)的电极电位分布图可知,大多数单电极的电位保持一致,且单电极间的电位波动较小。这可能是因为在浸泡初期,SRB不均匀吸附在电极表面,使得所形成的微生物膜分布不连续、不均匀,因而使微生物腐蚀主要发生在局部区域(微生物膜下),从而造成初期单电极间腐蚀电位极差值较大;浸泡中后期随着SRB的大量繁殖和在电极表面的吸附,附着在电极表面的微生物膜逐渐增厚并趋于均匀,最终使丝束电极的各个单电极上全面覆盖基本一致的微生物膜,造成微生物膜下较为均匀的微生物腐蚀,因此使浸泡后期各单电极电位基本保持不变。
3、结论
(1)在含菌溶液中浸泡14 d的黄铜挂片表面覆盖有明显的微生物膜,EDS分析显示主要元素为碳,另外还有一定的金属氧化物和硫化物。
(2)电化学阻抗谱结果表明,在无菌溶液中黄铜电极的电荷转移电阻Rct随着浸泡时间的延长而略有增大,说明电极耐蚀性能的增强;在含菌溶液中黄铜电极的电荷转移电阻Rct则随浸泡时间的延长而减小,说明含菌溶液中电极腐蚀反应的阻力随时间而减小。
(3)极化曲线显示,含菌溶液中电极的腐蚀电流密度明显大于无菌溶液中;无菌溶液中黄铜电极的腐蚀电流密度随浸泡时间的延长逐渐减小,而在含菌体系中电极腐蚀电流密度随浸泡时间的延长显著增大,浸泡14 d的腐蚀电流密度比浸泡1 d时增大到8倍以上。
(4)浸泡初期含菌溶液中丝束电极的单电极腐蚀电位极差值较大,最大为28 mV;随着浸泡时间的延长,丝束电极单电极间腐蚀电位极差值逐渐减小,150 h后减小到2 mV左右并基本稳定。浸泡初期电极表面发生局部区域的腐蚀,浸泡后期发生较为均匀的微生物腐蚀。
 相关新闻
相关新闻