热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
研究简介:心肌缺血再灌注损伤常见于心脏血流恢复后,如在心脏病发作后的血液再通或心脏手术后。这种损伤会导致组织破坏,可能引起心力衰竭。损伤的一个主要原因是活性氧自由基(ROS)的过度产生,特别是在再灌注的最初几分钟内。ROS的产生触发线粒体通透性过渡孔的开放,导致细胞死亡程序、微血管功能障碍和炎症级联反应。氢气(H2)作为一种抗氧化剂,已经显示出在预防和治疗缺血再灌注引起的致命损伤方面具有巨大潜力。H2具有选择性减少细胞毒性ROS的能力,同时不影响代谢氧化还原反应或破坏其他ROS参与的细胞信号传导。H2能够穿透生物膜,快速扩散到细胞质、线粒体和细胞核中,有效减少细胞毒性自由基。此外H2是一种对人类安全、无明显副作用的气体。尽管氢气的治疗效果已被广泛证明,但将其应用于临床治疗仍面临挑战。主要问题包括H2在水、盐水或血液中的溶解度低,导致其在血液和受损组织中的生物利用度较差。此外,H2的易燃性在制备含H2配方时造成了困难和安全隐患。因此开发新的、安全的H2传递系统以有效治疗具有重要意义。微泡是小的充气微球,通常用于超声诊断中作为对比增强剂。MBs也是重要的药物传递载体,可以在血液循环中稳定携带药物,并具有多种治疗应用。药物可以加载到MB壳上、嵌入到壳矩阵中,或加载到内部空间中。MBs作为封装治疗性气体的载体,为提高H2的生物利用度提供了新的可能性。本研究人员开发了一种超声可视的H2传递系统,通过将H2装载在微泡内(H2-MBs)来预防心肌缺血再灌注损伤。这种系统可以在常温和常压条件下大大提高单位体积中的H2浓度,并且H2-MBs可以在超声成像系统中进行可视跟踪,有效释放其治疗气体。提供了一种新的方法来提高氢气在生物医学应用中的有效性,特别是在预防心肌缺血再灌注损伤方面。通过使用H2-MBs,研究人员能够克服H2溶解度低和生物利用度差的问题,同时利用超声成像技术实现对H2输送的实时监控。
Unisense微电极研究系统的应用
使用Unisense氢气微电极在体外(磷酸盐缓冲盐溶液)和体内(大鼠心脏)环境中测量了从微泡中释放的H2的浓度。使用针式H2传感器(Unisense)在磷酸盐缓冲盐溶液(PBS)和血液中测量H2释放曲线。简要地说,向5mL PBS中加入0.2 mL H2-MBs或对照MBs(载体)。然后通过将针式H2传感器浸入MB悬浮液中并实时记录数据来确定H2释放曲线。对于体内H2释放曲线,将针式H2传感器插入五只健康大鼠的左心室(动脉血),并通过静脉注射向大鼠注入2×1010 H2-MBs或对照MBs。然后连续记录血液中H2的浓度。开发了一种新颖的、图像引导的治疗性H2输送系统,简单易用,由此产生的H2-MBs极大地提高了单位体积溶液中的H2溶解度。更重要的是,H2-MBs可以被视觉跟踪,并用于保护心肌缺血再灌注损伤。研究为基于H2的治疗应用的临床转化提供了潜在解决方案。
实验结果
开发了一种新颖的、图像引导的治疗性H2输送系统,简单易用,由此产生的H2-MBs极大地提高了单位体积溶液中的H2溶解度。更重要的是,H2-MBs可以被视觉跟踪,并用于保护心肌缺血再灌注损伤。研究为基于H2的治疗应用的临床转化提供了潜在解决方案。
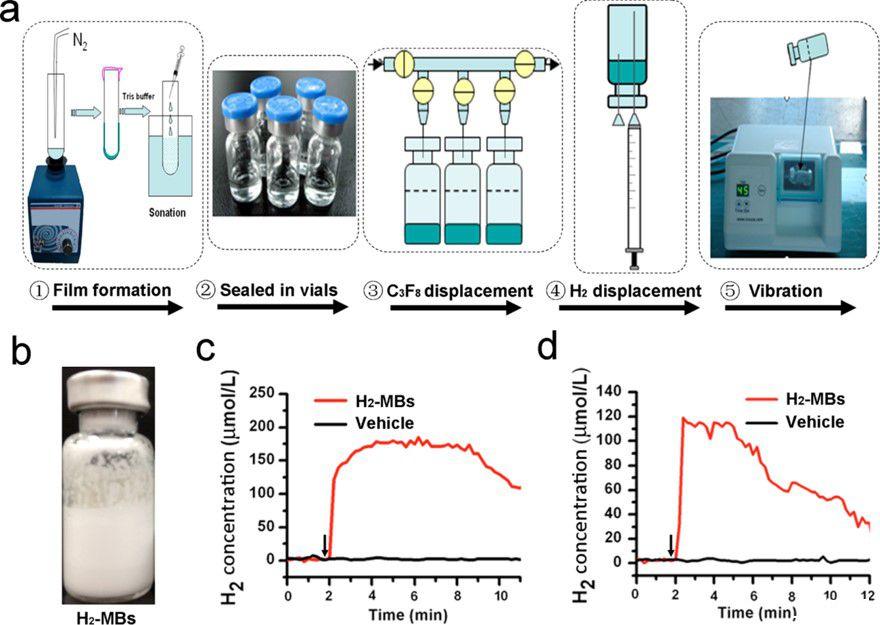
图1、H2-MBs的制备和表征。(a)H2-MBs制备的示意图。将由DSPC和DSPE-PEG2000(摩尔比=90:10)组成的15毫克磷脂混合物溶解在氯仿中。在形成膜和水合后,将含水分散液(脂质体)装入4 mL瓶中(每瓶1 mL),并用八氟丙烷(C3F8)置换瓶中的空气。随后,颠倒瓶子,并用注射器注入一定量的H2。因此,瓶子中挤出相等体积的C3F8。震动45秒后获得H2-MBs。(b)从上述方法中获得的H2-MBs的代表性图像(C3F8/H2比为1:1)。(c、d)体内外H2释放的代表性时间曲线。在体外实验中,将4×109 H2-MBs或对照MBs(载体)加入5 mL PBS中,并使用针式H2传感器检测来自MBs的H2释放。在体内实验中,将2×1010 H2-MBs或对照MBs静脉注射到大鼠体内,并使用针式H2传感器连续记录血液中的H2浓度,该传感器插入LV腔中(n=5)。箭头表示添加H2-MBs或对照MBs的时间。
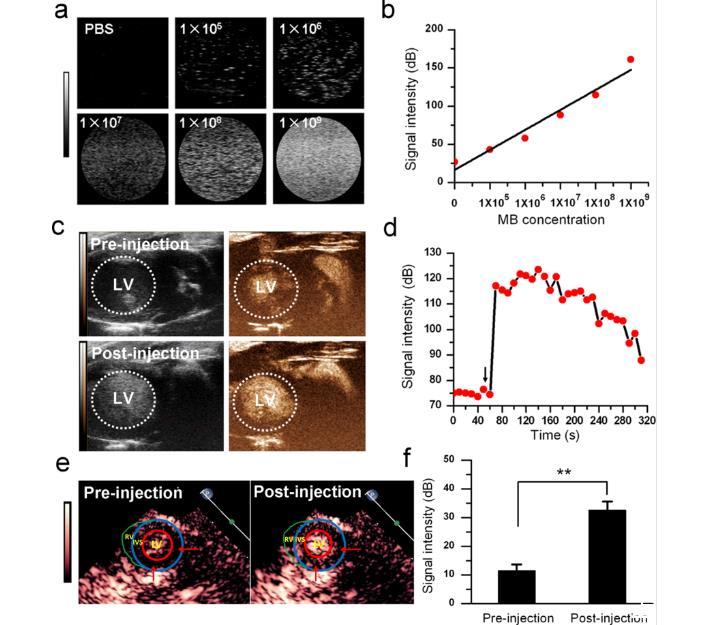
图2、H2-MBs的超声信号检测。(a)H2-MBs分散在各种浓度(5×105、5×106、5×107、5×108和5×109/mL)的PBS中的超声图像。使用Vevo 2100超声成像系统进行成像。(b)PBS中H2-MBs的超声信号强度的定量分析。(c)大鼠心脏LV中H2-MBs在静脉尾部注射H2-MBs前后的超声图像。使用Vevo 2100超声成像系统进行成像(n=3)。上排,注射H2-MBs前;下排,注射H2-MBs后;左侧面,B模式图像;右侧面,对比模式图像;LV,左心室(点线循环)。(d)H2-MBs注射进入大鼠后300秒的时间-强度曲线。箭头表示MB注射的时间。(e)大鼠心肌组织中H2-MB输送的超声图像。使用Philips IE33超声机进行成像。左侧,注射H2-MBs前;右侧,注射H2-MBs后;LV,左心室(红色循环);IVS,心室间隔(蓝色循环);RV,右心室(绿色循环)。箭头表示静脉注射H2-MBs后H2-MB输送到大鼠心肌组织中的情况。(f)H2-MBs的超声信号强度的定量分析。
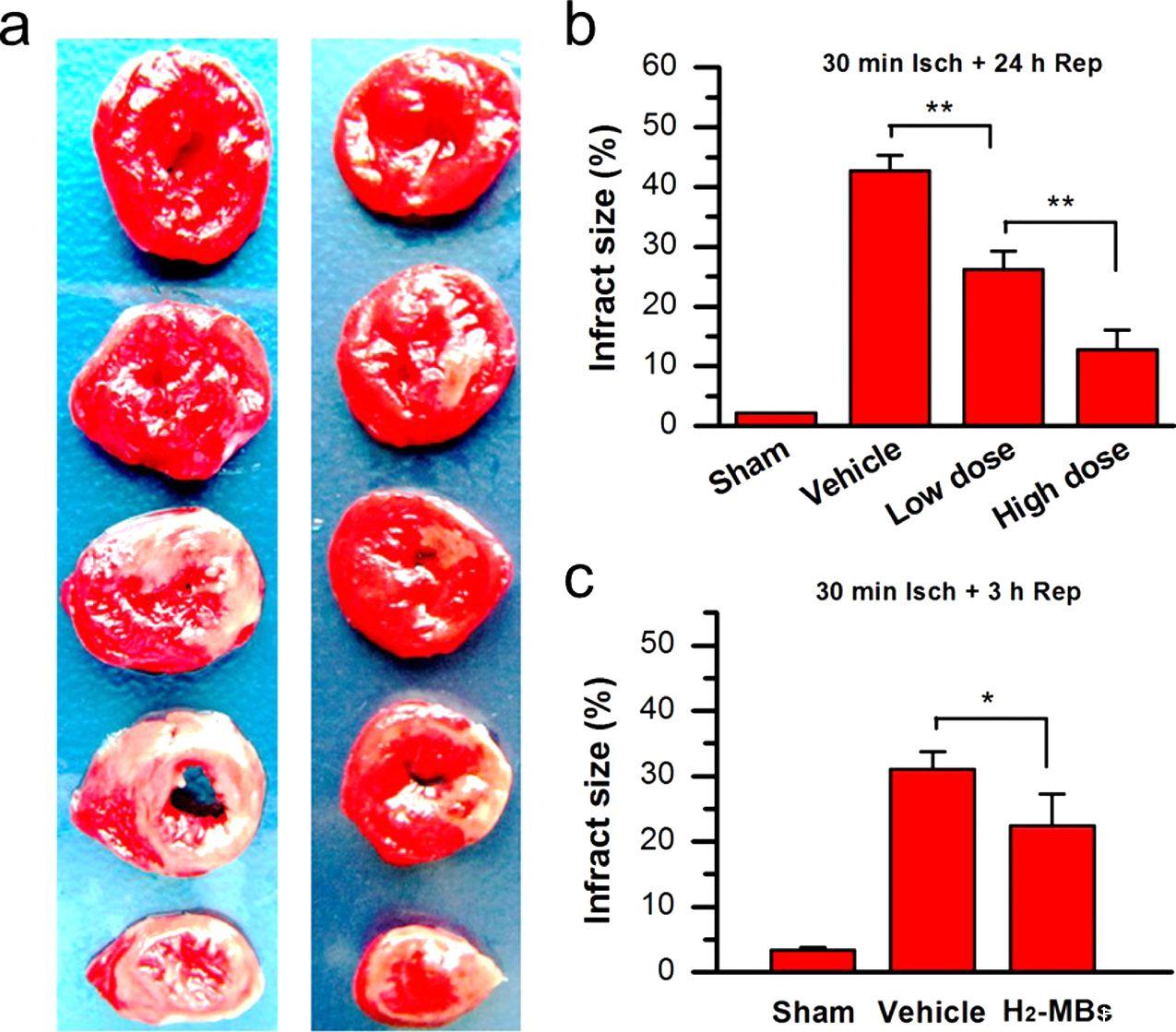
图3、H2-MBs预防心肌梗死。(a)给予对照微泡(左)或H2-MBs(右,高剂量)处理的大鼠经TTC染色的心肌连续切片的代表性图像。被染色阳性(红色)的组织代表活力心肌。未染色阳性(白色)的心肌代表梗死组织。(b)对于接受假手术处理的、接受车辆处理的或接受H2-MB处理的大鼠(低剂量,每只大鼠4×109气泡;高剂量,每只大鼠2×1010气泡)在LCA缺血30分钟和再灌注24小时后的心肌梗死面积的定量测定。接受H2-MB处理的大鼠显示出INF/LV显著减少(n=7)。*P<0.05,**P<0.01。数据表示平均值±s.d。(c)对于接受假手术处理的、接受对照MB处理的或接受H2-MB处理的大鼠在LCA缺血30分钟和再灌注3小时后的心肌梗死面积的定量测定;每只H2-MB处理的大鼠使用2×1010个H2-MBs。发现了类似的保护作用(n=5)。
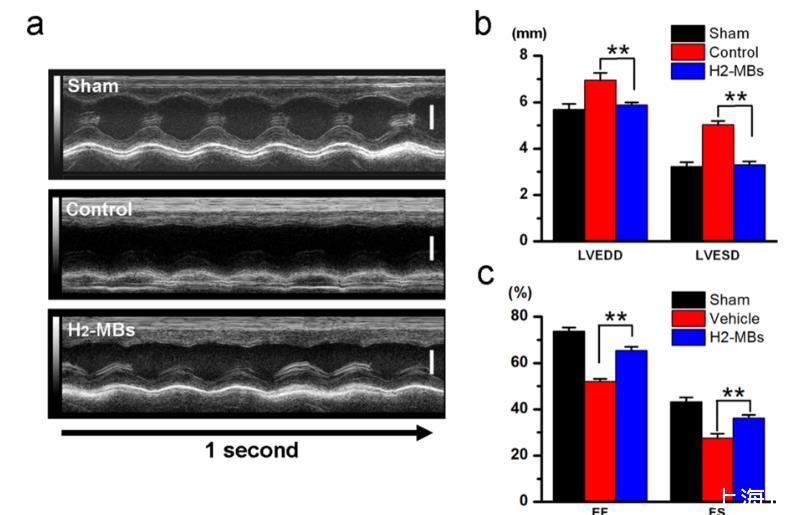
图4、H2-MBs减少不良的LV重塑。(a)接受假手术处理(假手术)、缺血再灌注对照微泡处理或缺血再灌注H2-MBs处理的大鼠的代表性M模式超声心动图像。对每组的M模式超声图像的测量是在缺血再灌注后48小时进行的。使用装备有MS-250扫描头探头的Vevo 2100系统进行成像,扫描速度为1000 Hz,频率为21 MHz。刻度条(垂直),4 mm。(b)基于超声心动图像,确定了LV尺寸,包括左室舒张末期直径(LVEDD)和左室收缩末期直径(LVESD)(n=5)。**P<0.01。数据表示平均值±s.d。(c)与对照组相比,H2-MB处理的大鼠的心脏收缩功能(FS%)和射血分数(EF%)显着改善(n=5)。
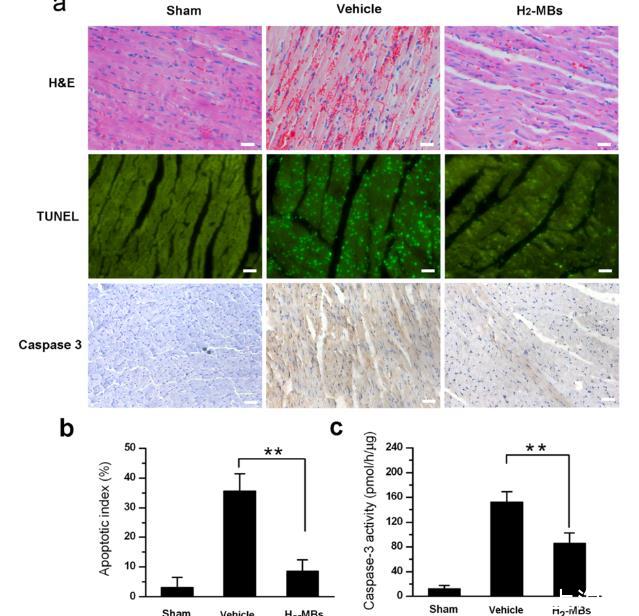
图5、H2-MBs保护心肌结构并减少心肌细胞凋亡。(a)来自接受假手术处理、车辆处理或H2-MB处理的大鼠的心脏切片的组织学分析,这些大鼠经过30分钟缺血和24小时再灌注;这些切片的H&E染色如图所示(上排)。接受对照微泡MB的大鼠心脏在缺血区显示明显出血和坏死(上排,中间),但H2-MBs处理的大鼠的心肌损伤减轻了(上排,右侧)。进行了TUNEL染色以检测心肌细胞的凋亡(中排),发现接受车辆MB的大鼠中TUNEL阳性细胞的数量显著增加(中排,中间)与接受假手术处理的大鼠相比(中排,左侧)。接受H2-MBs的大鼠显示TUNEL阳性细胞数量显著减少(中排,右侧)。进行了免疫组化染色以检测caspase-3的表达(下排),发现接受对照微泡MB的大鼠心肌中的caspase-3表达相对较高(下排,中间)与接受假手术处理的大鼠相比(下排,左侧)。接受H2-MBs的大鼠显示caspase-3表达减少(下排,右侧);刻度条=50μm。(b)通过计算五个高倍视野中TUNEL阳性核的百分比来绘制凋亡指数图,显示H2-MB处理的大鼠中TUNEL阳性核的数量显著减少与车辆组相比(n=5)。
结论与展望
缺血再灌注诱导的心肌细胞死亡是全球发病率和死亡率的主要原因。氢气(H2)作为一种抗氧化剂,已经显示出在预防和治疗缺血再灌注引起的致命损伤方面具有巨大潜力。然而由于H2在水中溶解度较低,在血液和受损组织中的生物利用度较差。研究者在研究过程中使用Unisense氢气微电极在体外(磷酸盐缓冲盐溶液)和体内(大鼠心脏)环境中测量了从微泡中释放的H2的浓度。这有助于了解H2-MBs(载氢微泡)释放H2的动态过程和速率。通过监测H2的释放情况,研究者能够评估H2-MBs在模拟的生理条件下(如PBS)以及在活体动物中的性能。这对于验证H2-MBs作为药物传递系统的有效性至关重要。在这里研究人员开发了一种超声可视的H2传递系统,通过将H2装载在微泡内(H2-MBs)来防止心肌缺血再灌注损伤。使用该系统可以在常温和常压条件下大大提高单位体积中的H2浓度。H2-MBs可以在超声成像系统中进行可视跟踪,并能有效释放其治疗气体。在缺血再灌注开始时在活体系统中输注H2-MBs会导致明显减小的梗死区大小和病理重塑。进一步分析表明,这种方法显著抑制了心肌细胞凋亡,并减少了心肌缺血再灌注大鼠中的心肌炎症和氧化损伤。这些结果表明,H2-MBs是一种有前途的H2基治疗应用的可视传递系统。本研究提供了一种新的方法来提高氢气在生物医学应用中的有效性,特别是在预防心肌缺血再灌注损伤方面。通过使用H2-MBs,研究人员能够克服H2溶解度低和生物利用度差的问题,同时利用超声成像技术实现对H2输送的实时监控。虽然Unisense微电极系统本身不提供成像功能,但它们测量的H2浓度数据可以用来验证超声成像观察到的H2-MBs分布和行为,为本研究提供了一种精确、可靠的工具来测量和监测H2-MBs释放的H2浓度,这对于评估这种新型药物传递系统的性能和潜力至关重要。
 相关新闻
相关新闻