热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
1.4分析项目及方法
COD采用重铬酸钾法测定;亚硝酸盐采用N-(1-萘基)-乙二胺光度法测定;硝酸盐采用紫外分光光度法测定;MLSS、MLVSS采用重量法测定;溶解性N2O利用丹麦Unisense微电极测定,测定前进行校准。N2O气体的采集:批式试验产生的N2O气体用氮气进行吹脱,使用50 mL注射器在反应器上部集气区采集气体样品,用气相色谱仪进行测定。气体分析与计算:利用PE600气相色谱仪对样品中的N2O浓度进行分析。N2O的释放速率和释放量参考Kong等、Kimochi等的方法进行计算。
2结果与讨论
2.1酸性进水条件下NO2-型反硝化的运行特性
课题组前期驯化得到适应酸性条件(pH=5.5)的NO2-型反硝化活性污泥,接种后再次降低进水pH至5.0并使其稳定,研究酸性条件下NO2-型反硝化的运行特性,并在80 d时分析了SBR反应器典型周期内C、N转化及N2O释放特性,结果如图1所示。由图1(a)可以看出,NO2-型反硝化在酸性条件下运行稳定。当初始pH为5.0时,出水NO2--N浓度为0~0.8 mg/L,其去除率大于99%;出水COD为33~51 mg/L,其去除率为86.1%~90.9%。经计算,去除的C/N在1.98~2.60之间。由图1(b)可以看出,随着反应的进行,NO2-和COD均随时间的增加呈降低趋势。经计算,NO2-的还原速率为10.88 mg/(gMLVSS·h),消耗的C/N为2.28。N2O的释放主要发生在前90 min,最大释放速率为58.27μg/(gMLVSS·min),有7.17%的NO2-转化为N2O,释放速率随时间呈先升后降的趋势。
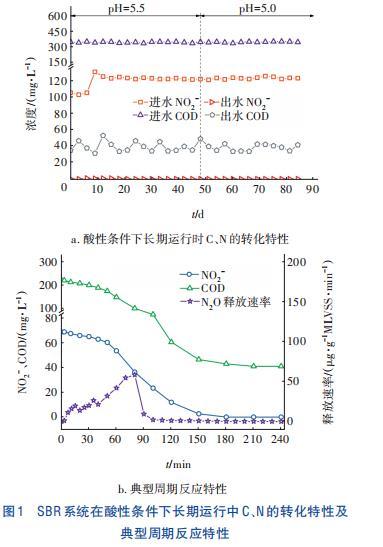
2.2 pH对NO2-型反硝化及N2O转化特性的影响
pH对C、N转化及N2O释放速率的影响如图2所示。可以看出,在不同pH条件下,NO2-和COD浓度均随时间的增加呈下降趋势,但反硝化速率不同。当pH为7.0时,60 min内完成了NO2-的还原,但N2O的释放主要发生在前30 min。随着pH由5.8降至5.0,出水NO2-浓度呈升高趋势。当pH为5.0时,NO2-去除率仅为43.3%。不同pH条件下,N2O释放呈现不同的特点。
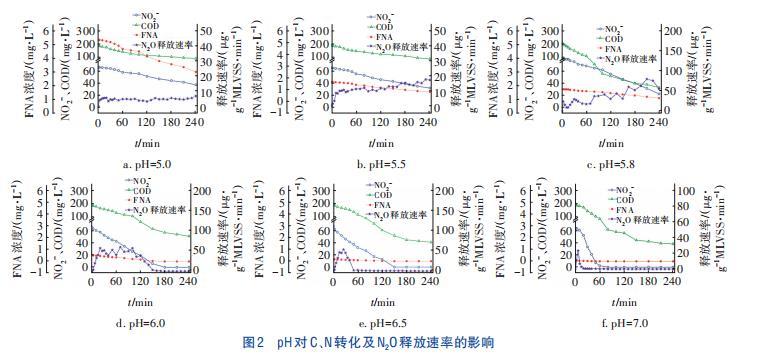
当pH分别为7.0、6.5时,N2O的释放速率随时间呈先升高后降低的趋势,且主要发生在反应前期,分别在第10、25分钟达到释放速率峰值。当pH为6.0时,N2O释放速率呈先升后降的趋势,在20~100 min保持较高的释放速率并出现了4个较明显的释放速率峰值。当pH≤5.8时,N2O释放速率随时间增加呈先上升后趋于稳定的趋势。从图3可知,酸性条件对NO2-还原速率及N2O释放量与转化率的影响显著。经计算,随着pH的降低,NO2-还原速率明显下降,pH为7.0时NO2-还原速率是pH为6.5的2.3倍。当pH降至5.0时,还原速率仅为7.0时的11.67%,表明酸性环境对反硝化具有抑制作用。
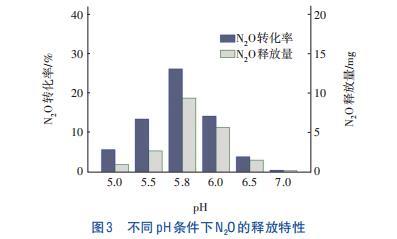
由图3可知,随着pH的降低,N2O转化率和释放量均呈先升高后降低的趋势,N2O转化率在pH为5.8时达到最大,为26.26%;当pH降至5.0时,N2O转化率降至5.78%。呈现这种规律的原因可能是,以NO2-为电子受体时,较低的pH对系统中NIR、NOR、NOS的活性产生了不同程度的影响。
彭永臻等的研究表明,pH对于以NO2-为电子受体的反硝化过程影响显著,除pH本身外,产生的FNA也会影响C、N的转化特性。由图3还可以发现,当pH由7.0降至5.0时,NO2-还原速率大幅降低,表明在酸性条件下NIR活性受到抑制,且pH越低抑制程度越严重。同时,酸性条件下NO2-的积累产生了较高浓度的FNA,然而N2O的释放量和转化率并未随着pH的降低呈单向升高的趋势,因此pH低于5.8时,很可能是pH及FNA对NOR的抑制更严重,导致N2O净产量下降。有研究报道,在以NO2-为电子受体时,FNA是N2O还原酶的主要抑制剂。因此,分析相同pH、不同FNA浓度条件下NO2-还原及N2O释放特征有助于探明FNA对NO2-型反硝化的影响。
 相关新闻
相关新闻