热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
2研究结果
2.1不同培养条件下沉积物孔隙水磷酸盐浓度变化
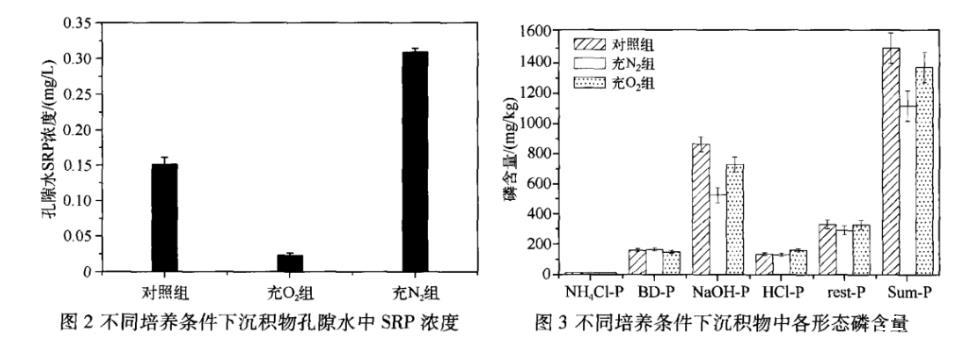
不同培养条件下,孔隙水中的SRP浓度表现为充N2组>对照组>充O2组(图2)。充N2组孔隙水SRP浓度约为0.309mg/L,是对照组的2倍左右,而充O2组的孔隙水SRP浓度仅为0.023mg/L.显然,厌氧使得沉积物孔隙水中磷酸盐浓度明显升高,而好氧条件下沉积物孔隙水磷酸盐浓度显著降低。
2.2不同培养条件下沉积物磷赋存形态变化
不同培养条件下,沉积物磷赋存形态变化如图3所示。充N2组和充O2组的沉积物总磷(Sum-P)含量与对照组相比均有不同程度的降低,且充N2组降低显著(降低了378.9mg/kg)。这种变化主要是由NaOH提取态磷(NaOH-P)和残渣态磷(rest-P)含量降低引起的。NaOH-P是红枫湖沉积物磷最主要的赋存形态,其含量约占总磷含量的57.8%,其次是rest-P,约占22.1%,其余20.1%为NH4Cl提取态磷(NH4Cl-P)、BD提取态磷(BD-P)和HCl提取态磷(HCl-P)。充N2条件下,NaOH-P含量明显减少,而孔隙水中SRP浓度有较大的升高(图2),说明NaOH-P释放进入孔隙水和上覆水。充O2条件下,沉积物总磷含量略有降低,NaOH-P含量略微降低是导致此现象的主要原因。与充N2条件不同的是,充O2条件下,沉积物孔隙水中SRP浓度(0.023mg/L)明显低于对照组(0.151mg/L)。
2.3不同培养条件下沉积物O2、H2S浓度以及pH值的剖面变化
不同培养条件下O2的渗透深度与浓度均为:充O2组>对照组>充N2组。自然条件下,沉积物O2的渗透深度约为2.1mm左右,界面O2浓度为137μmol/L.充N2培养条件下,界面O2浓度为70μmol/L,O2的渗透深度降低至0.9mm左右。而充O2培养之后,O2的渗透深度变为4.2mm,约为自然状态的2倍(图4a)。
自然、充O2以及充N2条件下,沉积物内部产生的H2S浓度存在较大差别。自然条件下,H2S在沉积物约3mm处出现,随后浓度开始增加,到20.7mm处达到峰值(22.9μmol/L)。充O2条件下,H2S的出现深度为15.9mm,在33.9mm处达到峰值(9.0μmol/L)。充N2培养的沉积物中,H2S的变化范围最大:从沉积物表面便开始产生H2S,并且随着深度增加H2S快速增加,在6mm深度处H2S浓度达到峰值(47.3μmol/L),随后伴随深度的增加出现少许波动,至12mm处开始下降(图4b)。
不同氧化还原条件下沉积物pH值也存在明显差异。3种条件下沉积物pH值在4.2mm处发生交叉。4.2mm处的pH值为6.9;4.2mm以上沉积物pH值均大于6.9,且大小顺序为:充O2组>对照组>充N2组;而4.2mm以下pH值均小于6.9,且顺序为:充N2组>对照组>充O2组(图4c)。
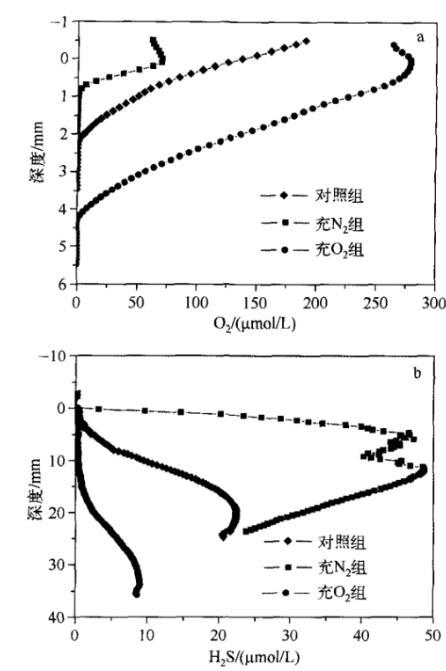
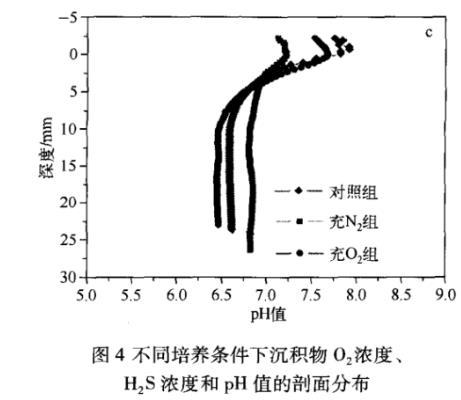
图4不同培养条件下沉积物O2浓度、H2S浓度和pH值的剖面分布
3讨论
3.1溶解氧对沉积物NaOH-P释放的影响
已有研究表明,溶解氧主要通过影响NaOH-P而影响沉积物内源磷的释放。NaOH-P是受铁铝金属氧化物约束的磷,该形态磷的沉淀与溶解是决定沉积物内源磷释放与否的关键。韩伟明在西湖沉积物磷释放实验中发现NaOH-P是沉积物释放的主要磷赋存形态。红枫湖沉积物中NaOH-P在总磷中所占比例最高,平均为57.8%.对沉积物孔隙水中SRP浓度、沉积物磷形态以及沉积物内部O2和H2S剖面分布特征的对比分析表明:经过充N2培养的沉积物与自然状态下的沉积物相比,沉积物内部O2浓度和渗透深度都有了大幅降低,与此同时,孔隙水中SRP浓度明显升高,而沉积物磷形态中NaOH-P和总磷含量明显降低,其他沉积物磷形态未发生显著变化。这反映在沉积物内部O2浓度降低的情况下,沉积物中的总磷含量降低的原因主要是NaOH-P的释放,并因此导致孔隙水中SRP浓度升高。此外,O2浓度的降低使得沉积物内部H2S浓度的剖面特征发生显著变化,从界面开始,硫酸根还原产生大量的H2S,H2S与二价铁离子产生硫化亚铁沉淀,铁离子的减少使得束缚NaOH-P的能力降低,NaOH-P更易被释放到孔隙水中。
充O2条件下沉积物NaOH-P含量略有降低,这可能是曝气过程对沉积物造成了一定扰动,导致沉积物磷的少量释放。
3.2溶解氧对沉积物rest-P释放的影响
从图3可知,沉积物总磷含量的降低除了主要受到NaOH-P含量降低影响之外,rest-P的降低也是部分原因。沉积物rest-P主要为有机磷。随着深度的增加,O2浓度逐渐降低,直至为0,深度继续增加,H2S开始出现(图4)。当微生物的耗氧超过了O2在沉积物中的扩散速率时,微生物便开始利用其它氧化剂进行无氧呼吸,电子受体优先顺序依次为溶解氧、硝酸根离子、高价态铁锰、硫酸根离子。当电极监测到有H2S产生时,说明溶解氧、硝酸根离子以及高价态铁锰等已经被还原。在充O2条件下,好氧微生物占主导,微生物消耗大量的O2,同时pH值升高,而rest-P含量几乎没有变化,说明好氧微生物并不消耗有机磷。而在充N2条件下,厌氧微生物占主导,消耗硫酸根,产生了大量的H2S,使pH值降低,同时,rest-P含量降低,可能是厌氧微生物消耗了有机质,将有机磷转变为无机磷,进而释放到上覆水体。O2浓度决定好氧微生物与厌氧微生物的比例,因而影响有机磷的迁移转化。
3.3不同条件下沉积物O2的扩散通量
沉积物与上覆水之间的相互作用已经引起广泛关注,了解不同条件下氧气的分布,可以估算出氧气的扩散通量,进而可以对扩散边界层中的微生物分布和营养物质的迁移转化进行定量研究。自然状态下红枫湖沉积物O2的扩散通量为235.6nmol/(m2·s)(20.4mmol/(m2·d)),这与汪嘉宁等在青岛会场湾所测得的O2的扩散通量(15.4——53.6mmol/(m2·d))接近,而充N2状态下,沉积物O2扩散通量仅为29.4nmol/(m2·s)(2.5mmol/(m2·d)),略低于王敬富等在红枫湖大坝自然缺氧状态下测出来的O2扩散通量(7.65mmol/(m2·d)),这可能是由于人工制造的厌氧程度本身就要高于自然界的厌氧程度。自然状态下沉积物O2的扩散通量为充N2条件下的近8倍,而充O2条件下沉积物O2扩散通量远远高于充N2条件。在沉积物~水界面处,充O2条件下微生物的耗氧活动和有机物的降解要比充N2条件下更加剧烈,但好氧环境下微生物活动对磷的吸收使得有机磷并未明显释放,而厌氧环境下微生物活动则显著促进了磷的释放。这表明好氧微生物和厌氧微生物对沉积物有机磷的影响存在重要差别。
红枫湖溶解氧的渗透深度为充O2组>对照组>充N2组。龚春生等对不同溶解氧水平下的底泥研究发现,沉积物间隙水中的好氧层会随上覆水溶解氧浓度的增大而增厚,好氧层的增厚会加大沉积物与上覆水之间的物质传输阻力。充O2状态与充N2状态相比,其沉积物具有更厚的好氧层,因而抑制了内源磷的释放。Vopel等发现即使没有光或者光很弱,沉积物表面的微生物垫也能产生氧气,因此在自然、充O2或者充N2状态下,氧气剖面均出现典型的界面放氧现象。虽然整个实验过程是在避光环境下开展的,但由于实验过程需要每天充气,因此实验室并不能保持始终黑暗,微生物垫表层应该也产生了一定量的O2.在自然、充O2或者充N2状态下,沉积物~水界面都存在上覆水复氧与微生物垫产氧,但三者溶解氧的走势存在明显差异:在自然状态下均匀下降,而充O2和充N2状态下,溶解氧在刚接触沉积物~水界面时呈升高的趋势,而后才逐渐降低。
4结论
1)厌氧条件下红枫湖沉积物TP含量显著降低,且主要是NaOH-P和rest-P含量降低所致,厌氧条件下沉积物孔隙水中磷酸盐浓度明显升高,而好氧条件下沉积物孔隙水磷酸盐浓度显著降低,表明厌氧条件显著促进了红枫湖沉积物磷释放。
2)厌氧条件下沉积物含氧量下降、硫还原活动强烈是导致NaOH-P释放的主要原因。微电极分析结果表明,与对照组相比,厌氧条件下界面O2浓度降低至70μmol/L(对照组为137μmol/L),氧渗透深度降低为0.9mm(对照组为2.1mm),H2S浓度升高至47.3μmol/L(对照组为22.9μmol/L)。O2浓度的降低加速了沉积物磷酸盐的还原作用并产生大量H2S,进而与二价铁离子形成硫化亚铁沉淀,最终导致NaOH-P(Fe-P)释放到孔隙水中。
3)好氧向厌氧条件的转换可通过改变沉积物内部pH值分布和微生物活动,促使rest-P(有机磷)减少。微电极分析结果表明,好氧条件下,rest-P含量几乎没有变化,而厌氧条件下,厌氧微生物不仅可以消耗硫酸根产生H2S,导致pH值降低,还可消耗有机质,将有机磷转变为无机磷。O2浓度决定了好氧微生物与厌氧微生物的比例,因而影响了有机磷的迁移转化。
4)沉积物~水界面氧化还原环境可影响沉积物氧渗透深度、pH值分布、微生物活动、硫循环以及有机质降解过程,进而控制沉积物磷的形态转化与释放。
5)联合应用微电极技术和沉积物磷形态分析对湖泊沉积物~水界面开展微尺度观测研究是揭示沉积物内源磷释放机制与控制因素的有效途径,但前者分辨率为mm-μm级尺度,而后者分辨率为cm级尺度,如何进行更有效的衔接和对比研究值得今后继续探索。